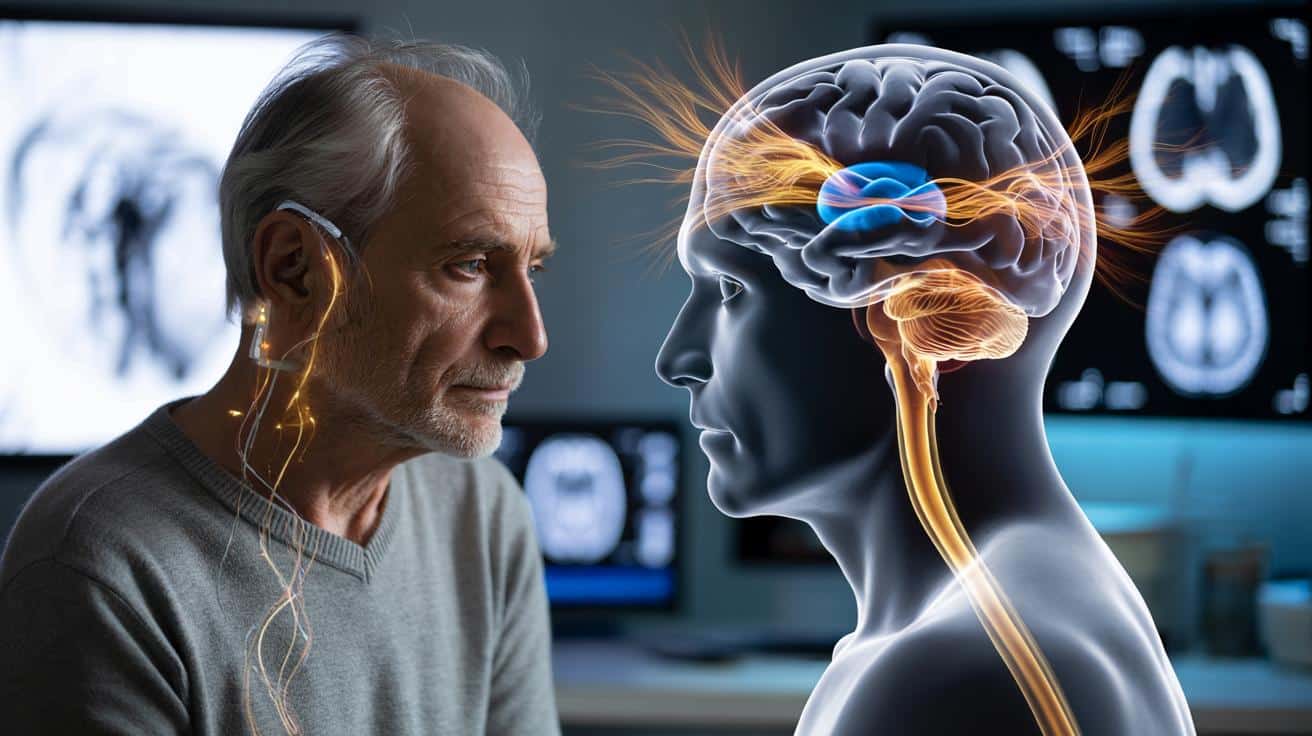
Przełom w walce z Alzheimerem? Lekarze testują „reset” nerwu błędnego
Naukowcy coraz śmielej sięgają po naturalne mechanizmy organizmu w walce z chorobami neurodegeneracyjnymi. Nerw błędny — najdłuższa nerwowa autostrada biegnąca od mózgu przez szyję aż do jelit — okazał się kluczem do ukrytych rezerw mózgu. Jego stymulacja może pobudzać „niebieską plamę” (locus coeruleus), która produkuje noradrenalinę — fundamentalny neuroprzekaźnik dla pamięci i koncentracji. U pacjentów z wczesnym Alzheimerem i łagodnymi zaburzeniami poznawczymi widziano wyraźną poprawę.
Najważniejsze informacje:
- Pierwsze zmiany w mózgu związane z Alzheimerem mogą pojawiać się już około 30. roku życia
- Locus coeruleus to obszar mózgu najbardziej wrażliwy na chorobę — tracony jest tam nawet 55% neuronów
- Stymulacja nerwu błędnego zwiększa stężenie noradrenaliny — kluczowego neuroprzekaźnika dla pamięci
- 52 pacjentów z łagodnymi zaburzeniami poznawczymi poprawiło wyniki testów pamięci po 6 miesiącach stymulacji
- Stymulacja przezskórna (na uchu) aktywuje te same obszary mózgu co implanty chirurgiczne
- Metoda pozostaje eksperymentalna — trwają większe badania kliniczne
Neurolodzy coraz uważniej przyglądają się nerwowi błędnemu.
Jego pobudzanie może spowalniać osłabianie pamięci typowe dla choroby Alzheimera.
Nowe badania sugerują, że celowana stymulacja tego nerwu wpływa na głęboko położone ośrodki mózgu związane z pamięcią i uwagą. Naukowcy liczą, że w ten sposób da się wyhamować proces, który dziś uważamy za praktycznie nieodwracalny.
Dlaczego Alzheimer zaczyna się znacznie wcześniej, niż myślimy
W powszechnej świadomości Alzheimer kojarzy się z bardzo podeszłym wiekiem. Tymczasem pierwsze zmiany w mózgu mogą ruszyć już około trzydziestki. Dzieją się po cichu, długo bez żadnych widocznych objawów.
Szczególnie wrażliwy jest maleńki obszar pnia mózgu – locus coeruleus, nazywany czasem „niebieską plamą”. To właśnie tam zaczyna się gromadzić nieprawidłowa postać białka tau, która z czasem tworzy splątane struktury uszkadzające neurony.
W badaniach pośmiertnych w chorobie Alzheimera stwierdzano utratę około 55% neuronów w locus coeruleus, przy około 30% w łagodnych zaburzeniach poznawczych.
Co istotne, wiele danych wskazuje, że uszkodzenia w tym obszarze pojawiają się jeszcze przed klasycznymi objawami otępienia. Nowoczesny rezonans magnetyczny czuły na barwnik neuromelaninę pokazuje, że w łagodnych i umiarkowanych postaciach choroby część tej struktury jest wciąż zachowana. To otwiera pole do interwencji – o ile znajdziemy sposób, jak ją chronić.
Nerw błędny – cicha autostrada między organami a mózgiem
Nerw błędny to jedna z najdłuższych dróg komunikacyjnych w naszym organizmie. Biegnie od mózgu przez szyję i klatkę piersiową aż do jamy brzusznej, łącząc mózg z sercem, płucami i przewodem pokarmowym. Około 80% jego włókien przenosi informacje z ciała do mózgu.
Locus coeruleus otrzymuje od nerwu błędnego stałą porcję sygnałów. W odpowiedzi reguluje wydzielanie noradrenaliny – neuroprzekaźnika odpowiedzialnego za czujność, skupienie, uczenie się, pamięć, a także za część reakcji odpornościowych.
Noradrenalina z locus coeruleus działa jak wewnętrzny „wzmacniacz” mózgu – podkręca uwagę, ułatwia zapamiętywanie i pomaga tworzyć nowe połączenia neuronalne.
Gdy dochodzi do uszkodzenia tej struktury, spada poziom noradrenaliny. Mózg traci ważny mechanizm pobudzenia, gorzej radzi sobie z utrwalaniem informacji, słabiej hamuje stan zapalny w tkance nerwowej. To właśnie w tym miejscu pojawił się pomysł: skoro bezpośrednio leczyć Alzheimera jest bardzo trudno, może warto wzmocnić układy modulujące, do których mamy już techniczne narzędzia.
Jak działa stymulacja nerwu błędnego
Stymulacja nerwu błędnego nie jest całkowitą nowością. Od lat stosuje się implanty elektryczne u osób z lekooporną padaczką oraz ciężkimi depresjami, które nie reagują na standardowe terapie. U części z tych pacjentów lekarze zauważali przy okazji poprawę pamięci i koncentracji.
Mechanizm obserwowany w badaniach na zwierzętach wydaje się dość spójny. Po włączeniu stymulatora aktywują się włókna czuciowe nerwu błędnego. Sygnały trafiają do jąder w pniu mózgu, a stamtąd bezpośrednio do locus coeruleus. W efekcie rośnie stężenie noradrenaliny w kluczowych obszarach odpowiedzialnych za pamięć: w hipokampie i korze mózgowej.
Naukowcy widzieli w doświadczeniach na szczurach, że odpowiednio dobrane parametry impulsów zwiększają plastyczność synaptyczną. To zdolność komórek nerwowych do wzmacniania lub osłabiania połączeń w zależności od aktywności – biologiczny fundament uczenia się.
Co może dawać pobudzanie nerwu błędnego
- wzmocnienie konsolidacji wspomnień (łatwiejsze utrwalanie nowych informacji),
- poprawę uwagi i tzw. pamięci roboczej,
- zmniejszenie neurozapalnej reakcji w mózgu,
- wspieranie sieci neuronalnych zaangażowanych w procesy poznawcze.
Ważny jest też charakter aktywności locus coeruleus. Przy chorobach neurodegeneracyjnych jego praca bywa chaotyczna i przewlekle podwyższona. Stymulacja nerwu błędnego może przywracać bardziej pulsacyjny, „fazowy” tryb wyładowań, który sprzyja selektywnej uwadze i sprawnemu filtrowaniu bodźców.
Pierwsze dane od osób z zaburzeniami pamięci
Po doświadczeniach z padaczką i depresją przyszedł czas na osoby z łagodnymi zaburzeniami poznawczymi i z wczesnym stadium Alzheimera. Chodzi o moment, kiedy objawy są jeszcze dość subtelne: lekkie problemy z zapamiętywaniem nowych informacji, sporadyczne gubienie wątku, trudności w odnajdywaniu słów.
W jednym z badań wzięło udział 52 pacjentów w wieku 55–75 lat z rozpoznanymi łagodnymi zaburzeniami poznawczymi. Otrzymywali godzinę stymulacji dziennie, pięć dni w tygodniu, przez około pół roku. Testy neuropsychologiczne po tym czasie wykazały statystycznie istotną poprawę pamięci i ogólnej sprawności poznawczej.
Jeszcze bardziej zaawansowaną grupę stanowili chorzy z już rozpoznaną chorobą Alzheimera, u których wszczepiono pełnowymiarowy implant nerwu błędnego. Po roku obserwacji:
| Grupa pacjentów | Wynik po 12 miesiącach |
|---|---|
| Wszyscy chorzy z implantem (17 osób) | 7 osób poprawiło wyniki testów, a 12 osób utrzymało stan bez wyraźnego pogorszenia w porównaniu z początkiem |
Liczby są niewielkie, badanie otwarte, bez klasycznej grupy kontrolnej, więc nie pozwala to jeszcze na daleko idące wnioski. Dla lekarzy to jednak sygnał, że warto inwestować w większe, lepiej zaprojektowane próby kliniczne.
Nie tylko implanty: stymulacja przezskórna na uchu i szyi
Wszczepienie stymulatora wymaga operacji w znieczuleniu ogólnym i niesie ze sobą typowe ryzyko chirurgiczne. Szacuje się, że powikłania mogą dotyczyć od 9 do 17% pacjentów, a problemy techniczne wymagające kolejnej interwencji sięgają podobnych wartości.
Aby uniknąć zabiegu, naukowcy opracowali urządzenia do przezskórnej stymulacji nerwu błędnego. Elektrody umieszcza się na małżowinie usznej lub na szyi, w miejscach, gdzie przebiegają jego gałązki czuciowe. Pacjent odczuwa lekkie mrowienie lub dyskomfort, ale zabieg nie wymaga nacinania skóry.
Badania z wykorzystaniem rezonansu funkcjonalnego pokazują, że przezskórna stymulacja ucha aktywuje bardzo podobne obszary mózgu jak klasyczne implanty.
W jednym z nowoczesnych badań randomizowanych, z podwójnie ślepą próbą, osoby z łagodnymi zaburzeniami poznawczymi korzystały z takiego urządzenia przez kilka miesięcy. U grupy aktywnie stymulowanej odnotowano lepsze wyniki testów pamięci niż u osób, które korzystały z „udawanego” sprzętu.
Inne prace obejmowały zdrowe osoby starsze i młodych dorosłych. Zdarzało się, że już po jednej sesji poprawiała się pamięć robocza lub zdolność rozpoznawania wcześniej prezentowanych bodźców. Część zespołów nie potwierdziła jednak tych efektów, co pokazuje, jak istotny jest dobór parametrów impulsów, czasu trwania sesji i regularności zabiegów.
Na jakim etapie jesteśmy i czego jeszcze brakuje
Obecnie trwa kilka większych badań u osób z łagodnymi zaburzeniami poznawczymi oraz z wczesną chorobą Alzheimera. Okres obserwacji wynosi od 6 do 18 miesięcy. Celem jest odpowiedź na dwa kluczowe pytania:
- czy stymulacja spowalnia samo tempo choroby, a nie tylko chwilowo poprawia wyniki testów,
- jakie parametry i czas trwania terapii są najbardziej korzystne i bezpieczne.
Dotychczasowe dane są zbyt wczesne, by mówić o gotowej metodzie leczenia. Lekarze zwracają uwagę, że część pacjentów reaguje wyraźnie lepiej niż inni, co sugeruje wpływ wieku, stopnia zaawansowania choroby, współistniejących schorzeń, a może także indywidualnych różnic w budowie nerwu błędnego.
Szanse, ograniczenia i praktyczny kontekst dla pacjentów
Dla chorych i ich rodzin kluczowe jest pytanie: czy taka terapia będzie dostępna, kiedy, w jakiej formie i dla kogo. Na dziś stymulacja nerwu błędnego pozostaje procedurą eksperymentalną w kontekście Alzheimera. Można o niej myśleć raczej jako o potencjalnym dodatku do standardowego leczenia, a nie jego zamienniku.
Ważną zaletą jest istniejące już doświadczenie kliniczne z padaczką i depresją. Lekarze znają profil działań niepożądanych: chrypka, kaszel, uczucie ścisku w gardle, czasem zaburzenia rytmu serca. Zwykle da się je ograniczyć, regulując parametry impulsów. W wersji przezskórnej najczęstsze są miejscowe podrażnienia skóry czy chwilowy dyskomfort.
Równolegle trwają prace nad lekami celującymi w białko tau oraz amyloid, nad szczepionkami i nad terapiami komórkowymi. W tym kontekście stymulacja nerwu błędnego może stać się jednym z elementów szerszego pakietu działań, którego zadaniem będzie nie tylko hamowanie uszkodzeń, lecz także wzmacnianie ocalałych sieci neuronalnych.
Dla osób, które mają w rodzinie historię choroby Alzheimera, najważniejsze na dziś pozostają klasyczne strategie ochrony mózgu: ruch, zdrowa dieta, kontrola ciśnienia i cukru, dobra jakość snu, aktywność społeczna i regularne ćwiczenie umysłu. To one tworzą „grunt” pod ewentualne przyszłe terapie neuromodulacyjne – bo im zdrowszy mózg, tym większa szansa, że skorzysta z dodatkowego „dopalacza” w postaci stymulacji nerwu błędnego.
Jeśli ta metoda przejdzie pomyślnie przez kolejne fazy badań, może zmienić sposób, w jaki patrzymy na choroby neurodegeneracyjne: mniej jak na jednokierunkowe osuwanie się w demencję, bardziej jak na dynamiczny proces, który da się modyfikować, wykorzystując ukryte rezerwy i naturalne układy regulacyjne naszego organizmu.
Najczęściej zadawane pytania
Czy stymulacja nerwu błędnego jest już dostępna dla pacjentów z Alzheimerem?
Nie — to wciąż procedura eksperymentalna. Trwają większe badania kliniczne, które mają potwierdzić skuteczność i określić optymalne parametry terapii.
Jak stymulacja nerwu błędnego wpływa na mózg?
Pobudza nerw błędny, który przesyła sygnały do locus coeruleus w pniu mózgu. To zwiększa wydzielanie noradrenaliny — neuroprzekaźnika kluczowego dla pamięci, uwagi i uczenia się.
Czy są już jakieś wyniki badań?
Wstępne badania na 52 pacjentach z łagodnymi zaburzeniami poznawczymi wykazały statystycznie istotną poprawę pamięci po 6 miesiącach terapii. To obiecujące, ale potrzeba większych prób.
Czy stymulacja jest bezpieczna?
W wersji przezskórnej (na uchu/szyi) ryzyko jest niskie — możliwe podrażnienia skóry. Wersja implantowana niesie ryzyko chirurgiczne (9-17% powikłań), ale lekarze mają już doświadczenie z padaczką i depresją.
Wnioski
Dla osób z rodziną obciążoną Alzheimerem najważniejsze pozostają sprawdzone strategie ochrony mózgu: regularny ruch, zdrowa dieta, kontrola ciśnienia i cukru, dobry sen i aktywność społeczna. One tworzą fundament, na którym ewentualne przyszłe terapie neuromodulacyjne będą mogły działać. Jeśli stymulacja nerwu błędnego przejdzie pomyślnie badania, może zmienić nasze myślenie o chorobach neurodegeneracyjnych — z jednokierunkowej drogi w demencję na proces, który można modyfikować, wykorzystując naturalne układy regulacyjne organizmu.
Podsumowanie
Neurolodzy testują innowacyjną metodę walki z Alzheimerem — stymulację nerwu błędnego. Ta najdłuższa w organizmie droga komunikacyjna łączy mózg z sercem, płucami i jelitami, wpływając na ośrodek pamięci w mózgu. Wstępne badania na pacjentach z łagodnymi zaburzeniami poznawczymi pokazują obiecującą poprawę pamięci i koncentracji.