Przełom w leczeniu Alzheimera? Naukowcy tworzą „bojowe” komórki mózgu
Badacze testują nową metodę walki z chorobą Alzheimera: genetycznie modyfikują komórki mózgu, by same namierzały i usuwały szkodliwe złogi.
Najważniejsze informacje:
- Naukowcy opracowali koncepcję modyfikowanych genetycznie komórek mózgu, które potrafią samodzielnie namierzać i usuwać szkodliwe płytki amyloidowe.
- Technologia wykorzystuje zmodyfikowane receptory CAR, przenosząc podejście stosowane w onkologii na grunt neurologii.
- Obecne terapie przeciwciałami monoklonalnymi mają ograniczoną skuteczność i wiążą się z ryzykiem poważnych skutków ubocznych.
- Głównym wyzwaniem w terapii mózgu jest uniknięcie wywołania nadmiernego stanu zapalnego, który mógłby uszkodzić zdrowe neurony.
- Badania znajdują się obecnie na etapie przedklinicznym, a ich skuteczność potwierdzono głównie w modelach zwierzęcych i preparatach tkankowych.
- Terapia genowa w przyszłości może być rozszerzona na inne choroby neurodegeneracyjne, takie jak choroba Parkinsona czy Huntingtona.
Dotychczasowe leki jedynie delikatnie spowalniały rozwój choroby i wymagały skomplikowanego leczenia przeciwciałami. Teraz na horyzoncie pojawia się koncepcja, która zamiast „sprzątać z zewnątrz”, uzbraja własne komórki układu nerwowego, by atakowały patologiczne struktury odpowiedzialne za obumieranie neuronów.
Choroba Alzheimera – dlaczego tak trudno ją zatrzymać
Choroba Alzheimera to najczęstsza przyczyna otępienia u osób starszych. W mózgu chorego stopniowo zanikają połączenia między neuronami, co przekłada się na problemy z pamięcią, mową, orientacją i samodzielnością w codziennym życiu.
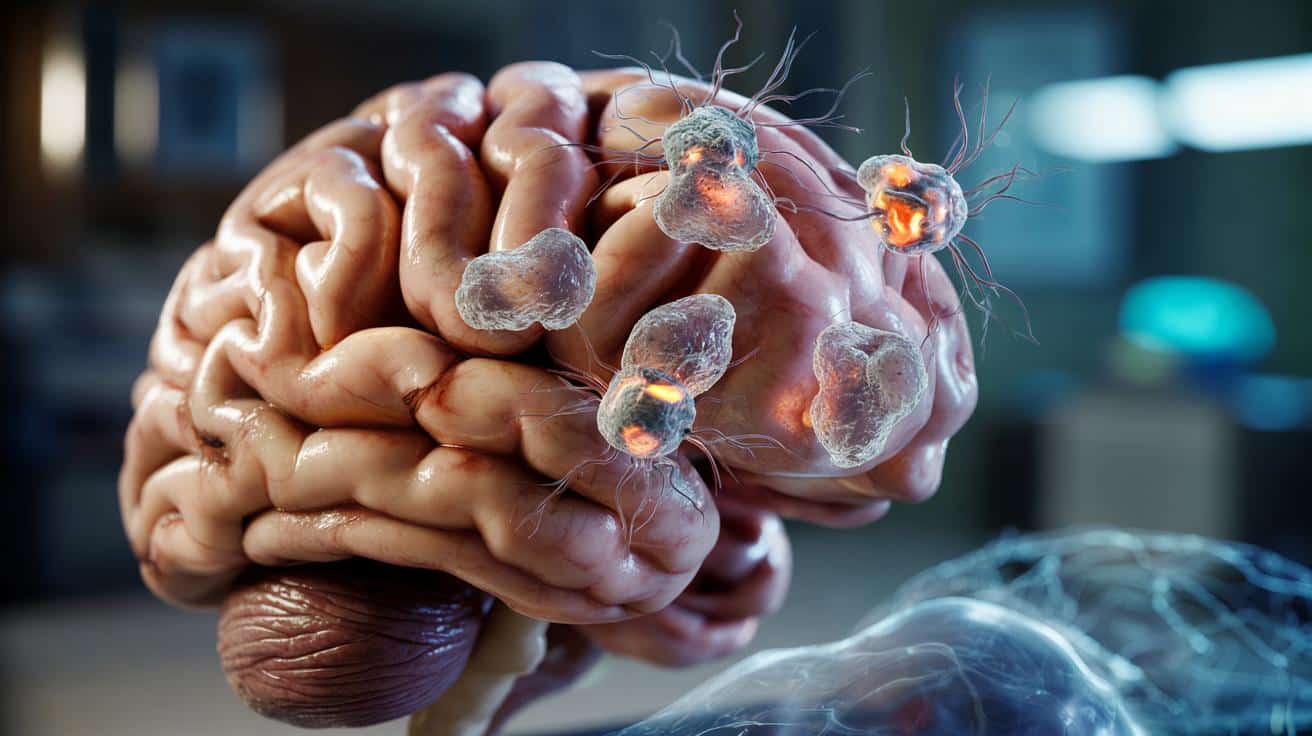
Od lat jednym z głównych „podejrzanych” pozostają tzw. płytki amyloidowe. To skupiska nieprawidłowego białka, które odkłada się w przestrzeniach między komórkami nerwowymi. Ich obecność wiąże się z zaburzeniem pracy całych sieci neuronów oraz z ich obumieraniem.
W ostatnich latach na rynek trafiły pierwsze leki zaprojektowane specjalnie po to, by usuwać te złogi. Są to przeciwciała monoklonalne – cząsteczki białkowe, które rozpoznają amyloid i pomagają go usuwać z mózgu. Badania pokazały, że takie leczenie może zmniejszyć ilość płytek i nieco spowolnić spadek funkcji poznawczych.
Nowe leki przeciwko chorobie Alzheimera po raz pierwszy skutecznie redukują ilość płytek amyloidowych w mózgu, ale ich działanie na objawy pozostaje umiarkowane, a ryzyko skutków ubocznych wciąż jest wysokie.
Przeciwciała pomagają, ale mają poważne ograniczenia
Terapie oparte na przeciwciałach oznaczają jednak dla pacjentów i lekarzy sporo problemów. Po pierwsze, wymagają dożylnych wlewów, często co kilka tygodni, w wyspecjalizowanych ośrodkach. Po drugie, aby lek był skuteczny, dawki muszą być wysokie, bo tylko ułamek trafia przez barierę krew–mózg do właściwego miejsca.
Największe obawy budzą skutki uboczne. U części pacjentów dochodzi do tzw. anomalii naczyniowych widocznych w badaniu rezonansem magnetycznym – obrzęku mózgu, drobnych krwawień. Dlatego terapię trzeba pod ścisłą kontrolą monitorować, a niektórym osobom ją przerywać.
Naukowcy szukają więc sposobu, by celować w płytki amyloidowe bardziej precyzyjnie, zużywając mniej leku i ograniczając niepożądane reakcje. Tutaj pojawia się pomysł wykorzystania koncepcji, która już zrewolucjonizowała leczenie niektórych nowotworów krwi.
CAR – technologia z onkologii przenosi się do neurologii
W leczeniu części białaczek i chłoniaków stosuje się od kilku lat tzw. terapię CAR. To skrót od Chimeric Antigen Receptor, czyli chimerycznego receptora antygenowego. Mówiąc prościej, lekarze pobierają od pacjenta komórki odpornościowe, modyfikują je genetycznie w laboratorium, a następnie podają z powrotem do organizmu.
Zmodyfikowane komórki noszą na swojej powierzchni specjalny receptor. Z jednej strony potrafi on bardzo precyzyjnie rozpoznać wybrany cel – np. białko występujące na komórkach nowotworowych. Z drugiej strony jego wewnętrzna część działa jak przełącznik „atakuj” i uruchamia silną odpowiedź komórki przeciwko temu celowi.
Technologia CAR polega na tym, że zamiast podawać gotowy lek z zewnątrz, lekarze przeprogramowują własne komórki pacjenta, by stały się żywym „lekiem”, stale patrolującym organizm.
Ta koncepcja fascinowała naukowców zajmujących się neurodegeneracją. Pojawiło się pytanie: czy da się tak „uzbroić” komórki związane z układem nerwowym, by samodzielnie czyściły mózg z płytek amyloidowych, bez zalewania go przeciwciałami?
Genetycznie modyfikowane komórki mózgu na celowniku płytek amyloidowych
Opisane w prestiżowym czasopiśmie naukowym badanie pokazuje pierwszą możliwą odpowiedź na to pytanie. Zespół badawczy wykorzystał koncepcję receptorów CAR, ale zamiast klasycznych komórek odpornościowych zastosował inne komórki związane z układem nerwowym.
Nowo zaprojektowany receptor osadzono w błonie komórkowej. Składa się on z dwóch głównych fragmentów:
- części zewnętrznej – rozpoznającej określony element płytki amyloidowej,
- części wewnętrznej – aktywującej komórkę i skłaniającej ją do „posprzątania” wykrytego złogu.
W praktyce takie komórki zachowują się jak wyspecjalizowane „mikroodkurzacze”: pływają w otoczeniu neuronów, wyłapują skupiska amyloidu, wiążą je i inicjują ich usuwanie. W modelach eksperymentalnych z użyciem tkanek mózgu i zwierząt laboratoryjnych badacze obserwowali zmniejszenie liczby płytek po wprowadzeniu zmodyfikowanych komórek.
Dlaczego mózg to szczególnie trudne pole działania
Naukowcy podkreślają, że nie można po prostu skopiować terapii z onkologii. Mózg jest znacznie wrażliwszy na stan zapalny niż np. krew czy węzły chłonne. Zbyt agresywna reakcja zmodyfikowanych komórek mogłaby uszkodzić neurony, które i tak są już osłabione przez proces chorobowy.
Dlatego konstrukcja receptorów CAR przeznaczonych do działania w tkance nerwowej musi być ostrożniejsza. Chodzi o to, by komórka skutecznie usuwała amyloid, ale nie wywoływała burzy zapalnej. W projekcie opisanym w pracy naukowej zastosowano tak dobrane elementy wewnętrznej części receptora, aby odpowiedź komórki była raczej „czyszcząca” niż destrukcyjna.
Na jakim etapie są prace nad „bojowymi” komórkami mózgu
Na razie to wciąż etap badań przedklinicznych. Oznacza to, że cała koncepcja była testowana głównie w modelach zwierzęcych i na preparatach tkankowych, a nie u osób z chorobą Alzheimera. Naukowcy sprawdzali m.in.:
| Etap prac | Co sprawdzano |
|---|---|
| Badania in vitro | Skuteczność wiązania amyloidu przez zmodyfikowane komórki i ich zdolność do usuwania złogów |
| Modele zwierzęce | Wpływ terapii na ilość płytek w mózgu oraz bezpieczeństwo długotrwałego działania |
Wstępne wyniki wyglądają obiecująco pod względem redukcji złogów, ale to jeszcze nie oznacza gotowego leku. Kolejnym wyzwaniem będzie udowodnienie, że usunięcie płytek faktycznie przekłada się na poprawę pamięci i funkcjonowania, a nie tylko na ładniejszy obraz w rezonansie czy biopsji.
Szanse i zagrożenia nowej terapii
Jeżeli taka metoda trafi kiedyś do praktyki klinicznej, może rozwiązać część problemów związanych z obecnymi terapiami. Zmodyfikowane komórki można by wprowadzić do organizmu raz lub kilka razy, licząc na to, że będą działać miesiącami jako żywy „serwis sprzątający”. To mogłoby zmniejszyć dawki podawanych leków i ograniczyć obciążenie dla organizmu.
Ryzyk jest jednak sporo. Główny lęk dotyczy nadmiernej aktywności komórek – gdyby zaczęły atakować nie tylko płytki amyloidowe, ale też zdrowe struktury, skutki mogłyby być bardzo poważne. Trzeba też mieć pewność, że wprowadzony materiał genetyczny nie ulegnie przypadkowym zmianom, które zmieniłyby zachowanie komórek w nieprzewidywalny sposób.
Każda terapia genowa działająca bezpośrednio w mózgu wymaga wyjątkowo długich i skrupulatnych badań bezpieczeństwa – od prostych modeli laboratoryjnych aż po ograniczone i ściśle monitorowane próby z udziałem ludzi.
Co ta koncepcja może oznaczać dla pacjentów w przyszłości
Eksperci z różnych ośrodków podkreślają, że nie należy spodziewać się takiej terapii w gabinetach neurologicznych w ciągu najbliższych kilku lat. Bardziej realistyczny scenariusz zakłada, że w pierwszej kolejności pojawią się niewielkie badania kliniczne z udziałem wybranych grup pacjentów, np. we wczesnym stadium choroby, poddanych bardzo ścisłemu nadzorowi.
Z czasem podobne podejście można byłoby rozszerzyć nie tylko na chorobę Alzheimera, ale też inne schorzenia neurodegeneracyjne, w których w mózgu gromadzą się patologiczne białka – jak w chorobie Parkinsona czy chorobie Huntingtona. W każdym przypadku wymagałoby to zaprojektowania osobnego receptora rozpoznającego inny typ złogów.
Dlaczego wciąż potrzebne są klasyczne metody wsparcia
Nawet jeśli terapie genowe staną się częścią leczenia Alzheimera, nie zastąpią całkowicie codziennych form wsparcia. Wczesna diagnostyka, aktywność intelektualna, rehabilitacja poznawcza, kontrola nadciśnienia, cukrzycy czy zaburzeń lipidowych nadal będą wpływały na tempo pogarszania się funkcji mózgu.
Dla rodzin osób chorych kluczowa pozostaje też opieka długoterminowa, dostosowanie mieszkania, organizacja dnia, edukacja na temat zachowań typowych dla otępienia. Zaawansowane terapie biologiczne nie rozwiążą tych praktycznych wyzwań, choć mogą wydłużyć okres względnej samodzielności chorego.
Warto też pamiętać, że płytki amyloidowe to tylko część całej układanki. W mózgu chorego pojawiają się inne zaburzenia, jak splątki białka tau, przewlekły stan zapalny czy zmiany naczyniowe. Jeżeli medycyna ma realnie zmienić przebieg choroby, najskuteczniejsze może okazać się łączenie różnych strategii – od nowoczesnych komórek CAR, przez przeciwciała, po leki wpływające na metabolizm białek i funkcję naczyń.
Nowa koncepcja modyfikowanych genetycznie komórek mózgu pokazuje, jak gwałtownie rozwija się biotechnologia stosowana do chorób uznawanych kiedyś za nieuleczalne. Dla pacjentów i ich bliskich ważna jest jedna wiadomość: choć Alzheimera nie da się dziś wyleczyć, kierunek badań zmienia się z biernego łagodzenia objawów na aktywną ingerencję w sam rdzeń procesów chorobowych.
Podsumowanie
Naukowcy testują nowatorską metodę leczenia choroby Alzheimera, wykorzystując zmodyfikowane genetycznie komórki mózgu działające podobnie do onkologicznej terapii CAR. Metoda ta ma na celu precyzyjne usuwanie toksycznych złogów amyloidowych, co może w przyszłości stanowić skuteczniejszą alternatywę dla obecnych terapii przeciwciałami.


Opublikuj komentarz