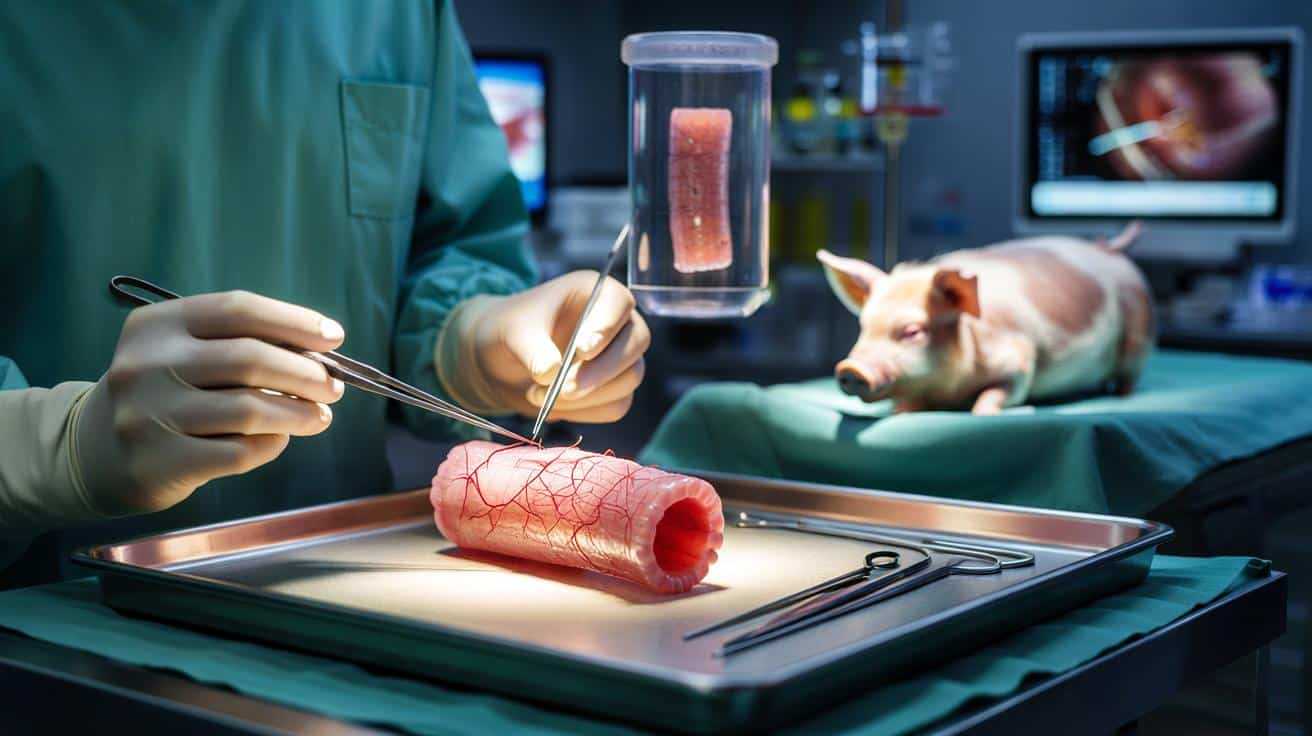
Przełom w laboratorium: naukowcy wyhodowali i wszczepili działający fragment przełyku
Eksperyment, w którym miniaturowe świnie odzyskały normalne połykanie po przeszczepie „uszytego na miarę” fragmentu przewodu pokarmowego, może całkowicie zmienić leczenie ciężkich wad wrodzonych i uszkodzeń przełyku.
Nowy etap medycyny rekonstrukcyjnej
Przełyk to nie tylko elastyczny kanał prowadzący pokarm do żołądka. To narząd, który musi prowadzić precyzyjne skurcze mięśni, odbierać i przekazywać sygnały nerwowe oraz wytrzymywać stałe obciążenia mechaniczne przy każdym kęsie. Zastąpienie go czymś sztucznym przez lata stanowiło ogromne wyzwanie.
Dlatego sukces zespołu z University College London uznano za kamień milowy. Naukowcy pokazali, że da się zbudować żywy, funkcjonalny fragment przełyku, który rośnie wraz z organizmem i zachowuje się jak naturalna tkanka, a nie jak obcy, martwy implant.
Badacze stworzyli biologiczną „rusztowanie” z tkanki zwierzęcej, zasiedlili je komórkami biorcy i uzyskali fragment narządu zdolny do prawidłowego połykania.
Jak zbudowano przełyk w laboratorium
Pierwszy krok polegał na pobraniu przełyku od świni. Z tkanki usunięto wszystkie komórki, pozostawiając wyłącznie tzw. macierz pozakomórkową, czyli naturalną, białkową konstrukcję organu. To ona zachowuje kształt i mikroarchitekturę narządu, a jednocześnie nie wywołuje silnej reakcji odpornościowej.
Przeczytaj również: 10 prostych ćwiczeń w domu, które odmienią twoją formę w 30 dni
Następnie do tak przygotowanego „szkieletu” wprowadzono komórki mięśniowe pochodzące od przyszłych biorców – mini-świń. Te komórki zostały wcześniej przeprogramowane do postaci komórek macierzystych o zwiększonej zdolności różnicowania, dzięki czemu mogły wytworzyć kilka typów tkanek potrzebnych w przełyku.
Całość umieszczono w biorreaktorze, czyli specjalnej komorze, w której można kontrolować temperaturę, skład pożywki, przepływ płynów i obciążenia mechaniczne. Przez tydzień komórki mogły się osadzać, łączyć i organizować w warstwy przypominające naturalny narząd. Pełny protokół przygotowania przeszczepu trwał około dwóch miesięcy.
Przeczytaj również: 10-minutowy trening na dół brzucha w domu: plan krok po kroku
Dwumiesięczne przygotowanie implantów mieści się w obecnych ramach leczenia dzieci z ciężką wadą przełyku, co czyni tę metodę realną kandydatką do wdrożenia.
Dlaczego wykorzystano świnie
Miniaturowe świnie są standardowym modelem w badaniach nad chirurgią i biomateriałami. Ich narządy mają rozmiar i budowę zbliżoną do ludzkich, a tempo wzrostu umożliwia ocenę, jak implant zachowa się w dynamicznie rozwijającym się organizmie.
W tym eksperymencie wybrano zwierzęta o masie około 10 kilogramów. To etap, w którym można porównać je do małych dzieci z wadami wrodzonymi przełyku – grupy, która w przyszłości może szczególnie skorzystać z takich terapii.
Przeczytaj również: Lekarze biją na alarm: viralny „sleep hack” z taśmą na usta może być groźny
Eksperyment na żywych zwierzętach: osiem świń, sześć miesięcy obserwacji
Chirurdzy usunęli u ośmiu mini-świń fragment przełyku o długości 2,5 centymetra. Zamiast niego wszyli laboratoryjnie wyhodowany segment narządu. Każdy implant osłonięto dodatkową, biodegradowalną siatką, która miała pobudzić tworzenie się naczyń krwionośnych i wzmocnić miejsce przeszczepu.
Przez pierwszy miesiąc obserwowano, czy zwierzęta przechodzą tzw. krytyczny okres po przeszczepie bez powikłań. Jak wynika z opisów, wszystkie świnie przetrwały ten etap bez groźnych komplikacji, przyjmowały pokarm i stopniowo wracały do normalnej aktywności.
Po trzech miesiącach wszczepione tkanki były całkowicie zintegrowane z otoczeniem, a pomiary wykazały prawidłowe ciśnienie potrzebne do przesuwania pokarmu do żołądka.
Według szczegółowych danych z sześciomiesięcznej obserwacji pięć zwierząt przeżyło do końca badania i odzyskało skuteczne połykanie. Badacze opisali w nich rozwój skurczowych włókien mięśniowych, sieci nerwów oraz sprawnego unaczynienia w obrębie przeszczepionego odcinka.
U części świń pojawiły się zwężenia w okolicy implantu, co utrudniało przechodzenie pokarmu. Zespoły medyczne poradziły sobie z nimi za pomocą zabiegów endoskopowych, takich samych jak te stosowane dziś u ludzi z bliznami i zwężeniami przełyku.
Co dokładnie udało się osiągnąć
| Element funkcji przełyku | Rezultat u świń |
|---|---|
| Skurcze mięśni | Zaobserwowano regularne, skoordynowane ruchy przesuwające pokarm |
| Nerwy | Przeszczepione odcinki wykształciły sieć nerwową reagującą na bodźce |
| Naczynia krwionośne | Rozwinęło się funkcjonalne unaczynienie, zapewniające odżywienie tkanek |
| Odporność na obciążenia | Implanty wytrzymywały codzienne obciążenia związane z karmieniem |
Droga do zastosowania u dzieci i dorosłych
Badacze nie ukrywają, że do wykorzystania tej technologii u ludzi wciąż potrzebne są kolejne etapy. Jednym z głównych zadań jest wydłużenie możliwego do odtworzenia fragmentu do 10–15 centymetrów. Tak długie segmenty byłyby potrzebne chociażby w ciężkich przypadkach wrodzonego braku przełyku lub po rozległych operacjach onkologicznych.
Najpoważniejsza bariera dotyczy ukrwienia. Im dłuższy fragment narządu, tym większy problem z dostarczeniem tlenu i składników odżywczych do każdej części. Bez stabilnej sieci naczyń implant nie przeżyje, a jego funkcja stopniowo zaniknie. Dlatego badacze testują różne sposoby projektowania naczyń w obrębie macierzy i przygotowywania przedsionków dla przyszłych zespoleń z istniejącymi tętnicami i żyłami pacjenta.
Równolegle trwa praca nad ujednoliceniem procesu produkcji. Celem jest stworzenie zestandaryzowanych „pustych” macierzy przełykowych pochodzenia świńskiego, które można będzie przechowywać i w odpowiednim momencie zaszczepić komórkami konkretnego pacjenta, na przykład dziecka z wadą wrodzoną.
- stała jakość każdego implantu, niezależnie od ośrodka, który go produkuje,
- mniej ręcznej pracy przy hodowli, a więcej automatyzacji i kontroli,
- możliwość przygotowania przeszczepu „na zamówienie” z komórek chorego,
- ograniczenie lub wyeliminowanie potrzeby stosowania leków immunosupresyjnych.
Szansa dla dzieci i dorosłych
Jeśli kolejne badania wypadną pomyślnie, ta metoda może pomóc kilku grupom pacjentów. Na pierwszym planie są dzieci z długoodcinkową atrezją przełyku, czyli ciężką wadą, w której fragment narządu w ogóle się nie wykształcił. Dziś lekarze próbują ratować sytuację, wykorzystując części żołądka lub jelita, co wiąże się z licznymi powikłaniami i często wymaga wielu operacji.
Drugą dużą grupę stanowią dorośli po leczeniu raka przełyku i osoby, które doznały rozległych oparzeń chemicznych po połknięciu substancji żrących. U nich uszkodzony odcinek narządu trzeba usuwać, a jego funkcję przejmują inne fragmenty przewodu pokarmowego. Bioinżynieryjny implant, oparty na własnych komórkach pacjenta, mógłby znacznie uprościć leczenie i dać lepszą jakość życia.
Szacuje się, że próby kliniczne na ludziach mogą ruszyć za trzy–cztery lata, jeśli kolejne testy bezpieczeństwa i skuteczności potwierdzą obecne wyniki.
Jak działa macierz pozakomórkowa i komórki macierzyste
Macierz pozakomórkowa to coś w rodzaju naturalnego „rusztowania” w każdym narządzie. Tworzą ją białka, włókna kolagenowe i inne składniki, które nadają tkankom kształt i wytrzymałość. Gdy usunie się z organu wszystkie komórki, macierz pozostaje jak pusty szablon, gotowy do zasiedlenia nowymi komórkami.
Gdy badacze wprowadzają do takiego szablonu komórki macierzyste lub przeprogramowane komórki pacjenta, korzystają one z mikroarchitektury macierzy jak z mapy. Dzięki temu łatwiej formują się w złożony narząd zamiast w przypadkową bryłę tkanki. To właśnie ta cecha pozwoliła odtworzyć nie tylko warstwę mięśniową przełyku, lecz także sieć nerwów i naczyń.
Z kolei użycie komórek wywodzących się z organizmu biorcy zmniejsza ryzyko odrzutu. Układ odpornościowy rozpoznaje je jako „swoje”, więc nie wymaga mocnej farmakologicznej blokady, jak w klasycznych transplantacjach narządów od dawcy.
Szanse, zagrożenia i pytania na przyszłość
Choć wyniki badań na świniach robią wrażenie, lekarze i bioetycy przypominają, że wprowadzenie tej metody do praktyki klinicznej musi przebiegać ostrożnie. Trzeba odpowiedzieć na szereg pytań: jak zachowa się implant po wielu latach, czy nie rozwiną się w nim niepożądane zmiany, jak często pojawią się zwężenia, a także czy proces hodowli będzie powtarzalny w setkach różnych szpitali.
Pacjenci i ich rodziny mogą natomiast liczyć na to, że rozwój bioinżynierii narządów stopniowo zmniejszy liczbę sytuacji bez wyjścia. W przypadku przełyku mówimy o strukturze położonej blisko dróg oddechowych i serca, więc każda poprawa bezpieczeństwa operacji ma ogromne znaczenie. Jeśli uda się dopracować tę technologię, za kilka lat w rozmowie z chirurgiem dziecięcym czy onkologiem pojęcie „wyhodowany przełyk z własnych komórek” może brzmieć już nie jak science fiction, lecz jak jedna z realnych opcji leczenia.