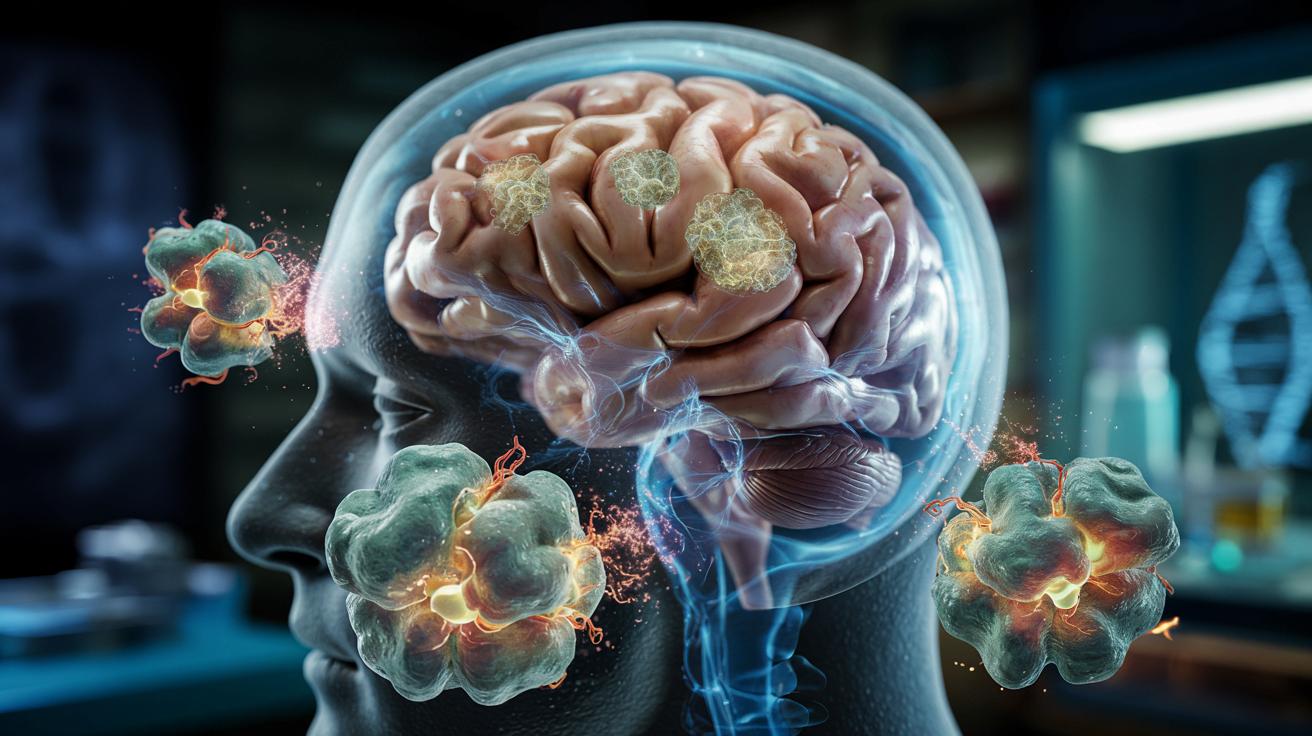
Alzheimer: genetycznie zmienione komórki mózgu jako nowa broń przeciw chorobie
Naukowcy testują przełomową metodę walki z chorobą Alzheimera, w której to komórki mózgu mają samodzielnie usuwać toksyczne złogi.
Dotychczasowe leki jedynie delikatnie spowalniały postęp otępienia i wymagały podawania dużych dawek przeciwciał. Teraz na horyzoncie pojawia się zupełnie inne podejście: precyzyjnie zaprogramowane komórki, które rozpoznają szkodliwe struktury w mózgu i rozprawiają się z nimi od środka.
Nowa era w leczeniu Alzheimera: komórki jak inteligentne leki
W 2025 roku wprowadzono na rynek trzy nowe terapie przeciw chorobie Alzheimera. Wszystkie skupiają się na jednym z najbardziej charakterystycznych elementów tej choroby: tzw. płytkach amyloidowych. Są to grudki białka beta-amyloidu, gromadzące się między neuronami. Badacze od lat podejrzewają, że zakłócają one przekazywanie sygnałów i przyczyniają się do obumierania komórek nerwowych.
Nowe leki z 2025 roku po raz pierwszy skutecznie zmniejszyły ilość tych złogów w mózgu, mierzoną w badaniach obrazowych. W praktyce przełożyło się to na lekkie spowolnienie pogarszania pamięci i funkcji poznawczych. Nie jest to więc cudowna terapia, lecz niewielki krok w stronę lepszego kontrolowania choroby.
Przeczytaj również: 3 proste nawyki, które naturalnie podkręcą twoje zdrowie po 50.
Problem w tym, że oparte są na przeciwciałach, które trzeba podawać w dużych dawkach dożylnie, zwykle co kilka tygodni. Taki sposób leczenia jest kosztowny, obciążający dla pacjenta, a do tego niesie ryzyko poważnych działań niepożądanych, jak obrzęki mózgu czy mikrowylewy widoczne w rezonansie magnetycznym.
CAR: technologia z onkologii wkracza do neurologii
W tym kontekście pojawia się zupełnie nowy pomysł, opisany w prestiżowym czasopiśmie naukowym. Chodzi o wykorzystanie technologii CAR, czyli receptorów chimerycznych, które zrobiły ogromną karierę w leczeniu niektórych rodzajów białaczki i chłoniaków. W onkologii metoda ta polega na tym, że naukowcy pobierają limfocyty T pacjenta, modyfikują je genetycznie w laboratorium, a następnie podają z powrotem. Tak przestrojone komórki rozpoznają komórki nowotworowe i je niszczą.
Przeczytaj również: Chiny jako pierwsze zgadzają się na sprzedaż implantu mózgu dla sparaliżowanych
Teraz podobny koncept próbuje się przenieść do chorób neurodegeneracyjnych. Zamiast polować na komórki rakowe, odpowiednio zaprogramowane komórki miałyby wyłapywać i usuwać złogi amyloidu w mózgu.
Nowa strategia polega na tym, by stworzyć komórkę, która pełni rolę celowanego „sprzątacza”: sama odnajduje toksyczne złogi białek i je usuwa, bez konieczności stałego podawania dużych dawek leku z zewnątrz.
Jak działa receptor chimeryczny w komórce mózgu
Receptor CAR to białkowa struktura wbudowana w błonę komórkową. Składa się z dwóch głównych części:
Przeczytaj również: 10-minutowy trening na dół brzucha w domu: plan krok po kroku
- fragmentu zewnętrznego – wystającego na powierzchnię komórki i rozpoznającego konkretną cząsteczkę, np. fragment beta-amyloidu,
- fragmentu wewnętrznego – znajdującego się w cytoplazmie i uruchamiającego odpowiedź komórki, gdy receptor „złapie” swój cel.
W onkologii, po związaniu antygenu nowotworowego, limfocyt CAR-T aktywuje się i niszczy komórkę rakową. W przypadku mózgu strategia może być inna: komórki wyposażone w takie receptory miałyby rozpoznawać złogi białkowe i inicjować ich rozkład lub usuwanie, na przykład poprzez nasilenie procesów „sprzątania” wewnątrz komórki albo pobudzenie sąsiednich komórek mikrogleju.
Dlaczego płytki amyloidowe stały się głównym celem
Choroba Alzheimera to złożona układanka, w której występują co najmniej dwa typy patologicznych białek: beta-amyloid oraz białko tau tworzące splątki wewnątrz neuronów. Część naukowców uważa, że amyloid jest pierwszym sygnałem zapalnym, który uruchamia kaskadę kolejnych uszkodzeń. Inni podkreślają, że usunięcie amyloidu nie zawsze przekłada się na spektakularne korzyści kliniczne.
Mimo tych sporów, płytki amyloidowe pozostają najbardziej oczywistym celem dla terapii biologicznych. Są stosunkowo łatwo wykrywalne w badaniach obrazowych i dają się dość precyzyjnie „namierzyć” przez przeciwciała czy receptory CAR.
| Cel terapii | Rola w mózgu | Wybrane metody działania |
|---|---|---|
| Płytki amyloidowe | Złogi między neuronami, podejrzewane o uszkadzanie połączeń | Przeciwciała, receptory CAR, małe cząsteczki wpływające na produkcję białka |
| Białko tau | Tworzy splątki wewnątrz neuronów, zaburza ich pracę | Przeciwciała anty-tau, eksperymentalne terapie genowe |
Genetycznie zmienione komórki mózgu – jak to ma wyglądać w praktyce
Opisany w pracy badawczej koncept polega na genetycznej modyfikacji komórek obecnych w ośrodkowym układzie nerwowym. Najczęstszym kandydatem są tu komórki glejowe, a szczególnie mikroglej – naturalne „służby porządkowe” mózgu. Te komórki już teraz usuwają obumarłe neurony i różne toksyczne cząstki, ale przy chorobie Alzheimera nie radzą sobie z nadmiarem patologicznych białek.
Naukowcy chcą więc tak przeprogramować mikroglej, aby dzięki receptorom CAR precyzyjniej rozpoznawał złogi amyloidu i reagował na nie bardziej zdecydowanie. Wstępne prace trwają głównie na modelach zwierzęcych oraz w hodowlach komórkowych.
Idea przypomina dołożenie bardzo czułego „radaru” do istniejącego systemu sprzątającego w mózgu, tak by nie przegapiać toksycznych struktur i usuwać je, zanim wyrządzą poważne szkody.
Przewagi nad tradycyjnymi przeciwciałami
W porównaniu z podawaniem przeciwciał, podejście oparte na komórkach niesie kilka potencjalnych korzyści:
- komórki po jednorazowym podaniu mogłyby działać miesiącami lub latami, bez konieczności ciągłych wlewów,
- działanie byłoby bardziej lokalne i celowane – komórki przebywają w tkance mózgowej i reagują tam, gdzie widzą złogi,
- mniejsze ryzyko ogólnoustrojowych działań niepożądanych, typowych dla wysokich dawek przeciwciał krążących w całym organizmie,
- możliwość elastycznego projektowania receptorów CAR tak, by jednocześnie rozpoznawały różne formy patologicznych białek.
Oczywiście jest to na razie scenariusz teoretyczny. Badacze muszą jeszcze sprawdzić, czy zmodyfikowane komórki rzeczywiście dotrą do odpowiednich obszarów mózgu, jak długo przeżyją oraz czy nie wywołają nadmiernego stanu zapalnego.
Ryzyka i znaki zapytania wokół takiej terapii
Brzmi to jak science fiction, ale praktyczne wdrożenie takiej terapii rodzi mnóstwo pytań. Po pierwsze, mówimy o genetycznej ingerencji w komórki ośrodkowego układu nerwowego – struktury wyjątkowo wrażliwej. Każde niekontrolowane pobudzenie układu odpornościowego w mózgu może skończyć się uszkodzeniem zdrowych neuronów.
Po drugie, wciąż nie ma pełnej zgody wśród badaczy co do tego, czy agresywne usuwanie amyloidu na późnych stadiach choroby przyniesie wymierną poprawę funkcji poznawczych. Część zmian w mózgu może być już wtedy nieodwracalna. Stąd rosnące zainteresowanie bardzo wczesną diagnostyką – jeszcze przed wyraźnymi objawami, gdy potencjalna terapia komórkowa miałaby większą szansę zahamować proces chorobowy.
Trzecia kwestia to bezpieczeństwo technik modyfikacji genetycznej. Do wprowadzenia genu kodującego receptor CAR w komórkach często wykorzystuje się zmodyfikowane wirusy. Ich zachowanie trzeba maksymalnie przewidzieć i kontrolować, aby uniknąć niepożądanych włączeń materiału genetycznego w newralgicznych miejscach.
Co to oznacza dla osób z grupy ryzyka
Dla pacjentów i ich rodzin pojawiające się informacje o kolejnych koncepcjach terapii bywają mylące. Z jednej strony rodzą nadzieje na skuteczniejsze leczenie, z drugiej budzą lęk przed zbyt śmiałymi eksperymentami na mózgu. Warto pamiętać, że badania nad komórkami z receptorami CAR w kontekście Alzheimera znajdują się na bardzo wczesnym etapie.
Zanim takie podejście trafi do badań klinicznych na ludziach, musi przejść przez szereg testów bezpieczeństwa i skuteczności na modelach zwierzęcych. Następnie czekają je wieloletnie, etapowe badania z udziałem pacjentów. O ile część osób ma nadzieję na szybkie wprowadzenie nowej terapii, realny horyzont czasowy to raczej wiele lat niż pojedyncze sezony.
Jakie działania mają sens już teraz
Mimo odległej perspektywy terapii komórkowych, osoby z podwyższonym ryzykiem choroby Alzheimera mogą zrobić kilka rzeczy już dziś, by zadbać o swój mózg. Badania epidemiologiczne wskazują, że na przebieg choroby wpływają czynniki stylu życia. Choć nie zastąpi to leczenia, może zmniejszyć ryzyko lub opóźnić początek objawów.
- regularna aktywność fizyczna – poprawia ukrwienie mózgu i wspiera plastyczność neuronów,
- dbanie o jakość snu – w czasie głębokiego snu mózg lepiej usuwa zbędne produkty przemiany materii,
- kontrola ciśnienia, cukrzycy i cholesterolu – choroby naczyniowe przyspieszają procesy neurodegeneracyjne,
- aktywność intelektualna i społeczna – nauka nowych rzeczy, rozmowy, kontakty z ludźmi sprzyjają tworzeniu zapasowych połączeń neuronalnych.
Warto też śledzić rozwój narzędzi diagnostycznych: testów płynów ustrojowych, badań obrazowych czy markerów genetycznych. Im wcześniej lekarze zauważą, że w mózgu dzieje się coś niepokojącego, tym większa szansa, że przyszłe terapie, w tym ewentualne leczenie komórkowe, przyniosą realną korzyść.
Technologia receptorów chimerycznych pokazała już swoją siłę w hematologii. Jeżeli uda się ją bezpiecznie zaadaptować do chorób mózgu, podejście do Alzheimera może się diametralnie zmienić: z biernego łagodzenia objawów w kierunku aktywnego „porządkowania” uszkodzonej tkanki nerwowej. Dla wielu rodzin zmagań z demencją to wizja, która choć odległa, daje poczucie, że medycyna nie stoi w miejscu i nie ogranicza się tylko do dobrze znanych schematów leczenia.