Nowe kolano bez protezy? Naukowcy pokazują dwie przełomowe metody
Przez dekady medycyna powtarzała, że zniszczona chrząstka stawowa to wyrok – nie odrasta, można jedynie łatać. Ta ponura wizja może się wkrótce zmienić. Dwóch niezależnych zespołów z USA – z Stanford Medicine i Northwestern University – zaprezentowało metody, które w testach laboratoryjnych faktycznie uruchamiają proces odbudowy chrząstki w kolanie. Jeśli wyniki potwierdzą się w badaniach na ludziach, miliony pacjentów z artrozą mogą uniknąć operacji wszczepienia protezy.
Najważniejsze informacje:
- Chrząstka stawowa prawie się nie regeneruje ze względu na brak własnego unaczynienia
- Enzym 15-PGDH rozkłada prostaglandynę E2 i przyspiesza starzenie chrząstki
- Blokada 15-PGDH zwiększyła produkcję chrząstki szklistej z 22% do 42% w badaniach na myszach
- Biomateriał z Northwestern tworzy nanowłókna imitujące strukturę naturalnej chrząstki
- Po 6 miesiącach od zastosowania biomateriału owcza chrząstka zawierała kolagen typu II i proteoglikany
- W USA artroza dotyka ok. 20% dorosłej populacji
- W Polsce z bólem stawów zmaga się kilka milionów pacjentów
- Zastrzyki zamiast operacji otwartej kolana mogą być przyszłością leczenia
W medycynie przez lata powtarzano, że zniszczona chrząstka stawowa nie odrasta. Teraz dwa niezależne zespoły badawcze podważają tę ponurą regułę.
Uczeni z renomowanych ośrodków w USA prezentują terapie, które w testach na zwierzętach i ludzkich tkankach uruchamiają proces odbudowy chrząstki w stawie kolanowym. Jeśli wyniki potwierdzą się w badaniach klinicznych, w perspektywie kilku lat część pacjentów może uniknąć ciężkiej operacji i wszczepienia protezy.
Dlaczego chrząstka w kolanie tak źle się goi
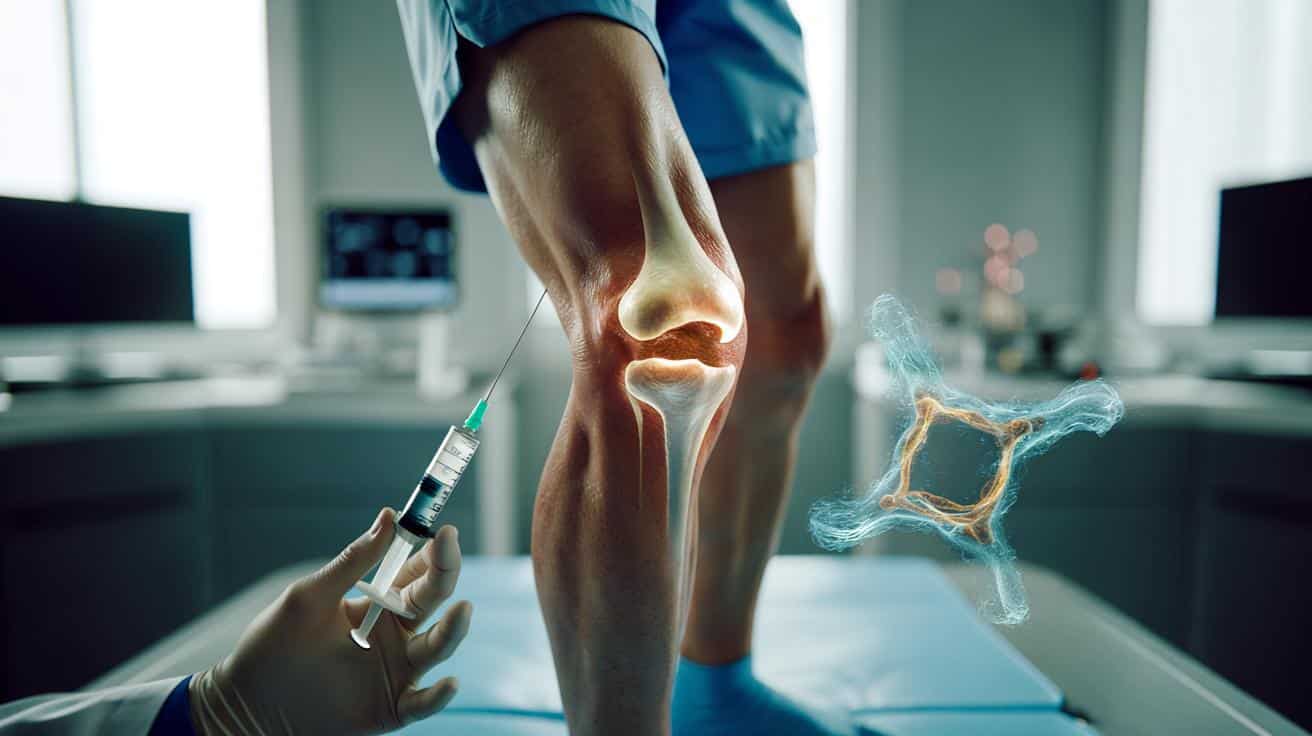
Chrząstka pokrywająca końce kości w stawie działa jak ślizgający się amortyzator. Jest twarda, gładka i świetnie znosi obciążenia, ale ma jeden ogromny minus – prawie się nie regeneruje. Nie ma własnego unaczynienia, a komórki chrzęstne dzielą się wolno i w ograniczonym stopniu.
Gdy dojdzie do urazu, wieloletniego przeciążenia albo zmian zwyrodnieniowych, w powierzchni stawowej pojawiają się „ubytki”, które organizm wypełnia gorszej jakości tkanką. To fibrochrząstka – mniej sprężysta, szybciej się ściera i z czasem pogłębia problem. Taki mechanizm leży u podstaw choroby zwyrodnieniowej stawów, czyli artrozy.
Obecnie większość pacjentów z zaawansowaną artrozą dostaje głównie leki przeciwbólowe i przeciwzapalne, a ostatecznym etapem leczenia jest wszczepienie endoprotezy stawu kolanowego.
Dla systemów opieki zdrowotnej to ogromne obciążenie finansowe, a dla chorych – długie miesiące bólu, ograniczeń i rehabilitacji. Nic dziwnego, że każde realne narzędzie do odbudowy chrząstki wywołuje tak duże emocje.
Blokada enzymu starzenia – odmładzanie chrząstki „od środka”
Pierwsza z prezentowanych metod powstała w Stanford Medicine. Naukowcy nie skupili się na przeszczepach czy komórkach macierzystych, ale na procesach starzenia zachodzących w samym stawie. Zidentyfikowali białko o nazwie 15‑PGDH, którego stężenie rośnie w chrząstce wraz z wiekiem.
Ten enzym rozkłada prostaglandynę E2 – cząsteczkę biorącą udział w naprawie tkanek. Gdy enzymu jest dużo, wewnętrzny „system serwisowy” stawu się rozkręca, a zdolność do regeneracji spada.
Co się stało, gdy zablokowano 15‑PGDH
Badacze wstrzyknęli do stawu kolanowego starszych myszy inhibitor 15‑PGDH. Po pewnym czasie przeanalizowali zachowanie chondrocytów, czyli komórek chrząstki. Okazało się, że ich aktywność genetyczna przesunęła się w stronę bardziej „młodzieńczego” profilu.
- odsetek komórek wytwarzających tzw. chrząstkę szklistą wzrósł z 22% do 42%
- liczba komórek tworzących słabszą fibrochrząstkę spadła mniej więcej o połowę
Innymi słowy, organizm przestawił się z trybu „łatania dziur byle czym” na tworzenie pełnowartościowej warstwy ochronnej.
Pierwsze sygnały z ludzkiej chrząstki
Aby sprawdzić, czy podobny efekt może wystąpić u ludzi, zespół sięgnął po fragmenty chrząstki kolanowej usunięte podczas standardowych operacji wymiany stawu. W kontrolowanych warunkach laboratoryjnych traktowano je tym samym inhibitorem 15‑PGDH.
Już po tygodniu terapii w ludzkiej chrząstce dało się zauważyć wczesne oznaki przebudowy w kierunku tkanki o lepszej jakości mechanicznej.
Dodatkową zachętą są wyniki wczesnej fazy badań klinicznych, w których sprawdzano bezpieczeństwo tego typu inhibitorów u zdrowych ochotników – nie odnotowano istotnych działań niepożądanych. To otwiera drogę do testów bezpośrednio w chorobowo zmienionych stawach.
„Inteligentny” żel w strzykawce – rusztowanie dla nowej chrząstki
Drugi kierunek prac rozwija zespół z Northwestern University. Tu kluczową rolę odgrywa nowy biomateriał, który po wstrzyknięciu do stawu ma zamienić się w coś w rodzaju rusztowania dla odrastającej chrząstki.
Materiał łączy dwa składniki: bioaktywny peptyd, czyli krótki fragment białka, oraz chemicznie zmodyfikowany kwas hialuronowy. Oba elementy łączą się samoistnie w nanowłókna przypominające strukturę naturalnej chrząstki.
Od gęstego żelu do sprężystej matrycy
Lekarze wprowadzają biomateriał w formie gęstego żelu bezpośrednio w miejsce ubytku. W kontakcie z jonami wapnia obecnymi w stawie żel zmienia się w miękką, porowatą matrycę. Do tak przygotowanego środowiska mogą migrować własne komórki pacjenta.
Technologię przetestowano na owcach z poważnymi ubytkami chrząstki w stawie porównywalnym do ludzkiego kolana. Po sześciu miesiącach w miejscu uszkodzenia zaczęła się formować nowa warstwa tkanki zawierająca:
- kolagen typu II – główne białko nadające chrząstce wytrzymałość na ściskanie
- proteoglikany – cząsteczki „wiążące wodę”, odpowiedzialne za elastyczność i amortyzację
To zestaw bardzo zbliżony do tego, który występuje w zdrowej chrząstce stawowej.
Czym różni się to od obecnych zabiegów
Dziś jedną z częściej stosowanych metod miejscowej naprawy chrząstki jest tzw. technika mikrozłamań. Chirurg nawierca drobne otwory w kości pod ubytkiem, żeby do miejsca uszkodzenia napłynęła krew i komórki. Zabieg bywa pomocny, ale wyhodowana w ten sposób tkanka często ma gorsze właściwości mechaniczne.
Nowy biomateriał ma skłaniać komórki do tworzenia chrząstki szklistej, bardziej odpornej na ścieranie i długotrwałe obciążenia niż fibrochrząstka powstająca po mikrozłamaniach.
Zespół kierowany przez Samuela Stuppa przygotowuje się obecnie do procedur dopuszczeniowych w amerykańskiej agencji leków FDA, co jest niezbędne, by rozpocząć pierwsze badania z udziałem ludzi.
Dwie drogi, jeden cel: odsunąć w czasie protezę
Obie metody działają w zupełnie inny sposób. W skrócie można je przedstawić tak:
| Strategia | Mechanizm | Główny cel |
|---|---|---|
| Blokada 15‑PGDH | usunięcie „hamulca” molekularnego związanego ze starzeniem, pobudzenie własnej regeneracji | odmłodzenie chrząstki bez dodatkowych materiałów |
| Biomateriał z kwasem hialuronowym | stworzenie specjalnego rusztowania, po którym rosną nowe komórki | prowadzenie odbudowy w miejscu dużego ubytku |
Łączy je dążenie do jednego efektu: zmniejszenia bólu i przywrócenia ruchomości stawu na tyle skutecznie, by pacjent jak najdłużej nie potrzebował endoprotezy. Biorąc pod uwagę, że artroza dotyka ogromnej części dorosłej populacji w krajach rozwiniętych, nawet częściowe powodzenie tych prac przełoży się na miliony ludzi.
Co to oznacza dla chorych na artrozę
W USA choroba zwyrodnieniowa stawów dotyczy mniej więcej jednej piątej dorosłych i generuje dziesiątki miliardów dolarów wydatków rocznie. W krajach europejskich skala problemu jest podobna – w samej Francji mówi się o ponad 10 milionach osób. W Polsce, według różnych szacunków, z bólem stawów o podłożu zwyrodnieniowym zmaga się kilka milionów pacjentów.
Jeśli nowe terapie przejdą pomyślnie przez pełną ścieżkę badań klinicznych, ich zastosowanie może wyglądać bardzo zwyczajnie: seria zastrzyków do stawu zamiast operacji z otwarciem kolana. Taki scenariusz brzmi jak medycyna przyszłości, ale pierwsze etapy już się dzieją.
Docelowo lekarz ortopeda mógłby dobrać metodę do pacjenta: u kogoś z wczesną artrozą zastosować blokadę enzymu, a przy większych ubytkach sięgnąć po biomateriałowe „rusztowanie”.
Co warto wiedzieć, zanim pojawi się nowy zastrzyk na kolano
Trzeba jednak pamiętać o kilku istotnych kwestiach. Po pierwsze, większość opisanych wyników pochodzi z badań na zwierzętach i z analiz tkanki w laboratorium. Człowiek jest znacznie bardziej skomplikowany – ma inne obciążenia, choroby współistniejące, leki. Nie wiadomo jeszcze, czy regeneracja będzie równie trwała jak w modelach zwierzęcych.
Po drugie, nawet najlepsza terapia nie zastąpi zdrowego trybu życia. Nadwaga, brak ruchu, źle dobrane obciążenia sportowe czy wieloletnia praca fizyczna dalej będą niszczyć stawy. Nowe metody mogą spowolnić skutki, ale nie unieważnią wszystkich czynników ryzyka.
Wreszcie, pojawia się pytanie o koszty i dostępność. Leki blokujące konkretne enzymy i zaawansowane biomateriały rzadko są tanie na starcie. W pierwszych latach mogą być zarezerwowane dla pacjentów z najbardziej nasilonym bólem lub tych, u których inne sposoby zawiodły. Z czasem, gdy patenty się kończą, technologie zwykle tanieją i stają się szerszej dostępne.
Jak pacjent z chorym kolanem może skorzystać z takiej wiedzy już dziś
Choć opisane terapie nie są jeszcze w standardzie, sama świadomość zmian w podejściu do chrząstki może wpłynąć na decyzje podejmowane wspólnie z lekarzem. Coraz większy nacisk kładzie się na jak najwcześniejsze wychwycanie objawów – ból przy schodzeniu po schodach, poranną sztywność, trzaski czy epizody „blokowania się” stawu.
Szybka konsultacja ortopedyczna, odpowiednio dobrana rehabilitacja, redukcja masy ciała i ćwiczenia wzmacniające mięśnie wokół kolana wciąż należą do najbardziej skutecznych i dostępnych działań. Jeśli w przyszłości do tego pakietu dojdą zastrzyki faktycznie odbudowujące chrząstkę, może się okazać, że wizja „jednej protezy w życiu” przestanie być dla wielu osób nieunikniona.
Najczęściej zadawane pytania
Czy nowe metody leczenia kolana są już dostępne dla pacjentów?
Nie, obie terapie są w fazie badań przedklinicznych. Badania na ludziach mają się rozpocząć po procedurach w FDA.
Na czym polega blokada enzymu 15-PGDH?
To inhibitor wstrzykiwany do stawu, który hamuje rozkład prostaglandyny E2 i uruchamia procesy regeneracji chrząstki.
Czy biomateriał z Northwestern działa tylko przy małych ubytkach?
Biomateriał jest przeznaczony do większych ubytków – tworzy rusztowanie, po którym migrują własne komórki pacjenta.
Ile czasu minie zanim terapie będą powszechnie stosowane?
Jeśli badania kliniczne się powiodą, pierwsze terapie mogą być dostępne za kilka lat.
Czy nowe metody zastąpią zdrowy styl życia w zapobieganiu artrozy?
Nie, terapie mogą spowolnić skutek, ale nie unieważnią czynników ryzyka jak nadwaga, brak ruchu czy przeciążenia.
Wnioski
Dla pacjentów z chorym kolanem to wciąż dobra wiadomość, nawet jeśli nowe terapie nie są jeszcze dostępne. Świadomość, że nauka nie stoi w miejscu, pozwala podejmować bardziej świadome decyzje z lekarzem. Już dziś warto dbać o wczesne objawy – konsultacja ortopedyczna, rehabilitacja, redukcja masy ciała i ćwiczenia wzmacniające mięśnie wokół kolana pozostają najskuteczniejszymi dostępnymi działaniami. Gdy do tego pakietu dojdą zastrzyki faktycznie odbudowujące chrząstkę, wizja jednej protezy w życiu może przestać być nieunikniona dla wielu osób.
Podsumowanie
Naukowcy z Stanford Medicine oraz Northwestern University przedstawili dwie innowacyjne metody leczenia zwyrodnienia stawów kolanowych bez konieczności wszczepiania protezy. Pierwsza terapia polega na blokowaniu enzymu 15-PDG, który przyspiesza starzenie chrząstki, druga wykorzystuje specjalny biomateriał tworzący rusztowanie dla regenerującej tkanki. Oba podejścia przeszły testy na zwierzętach i ludzkich tkankach, otwierając drogę do badań klinicznych.