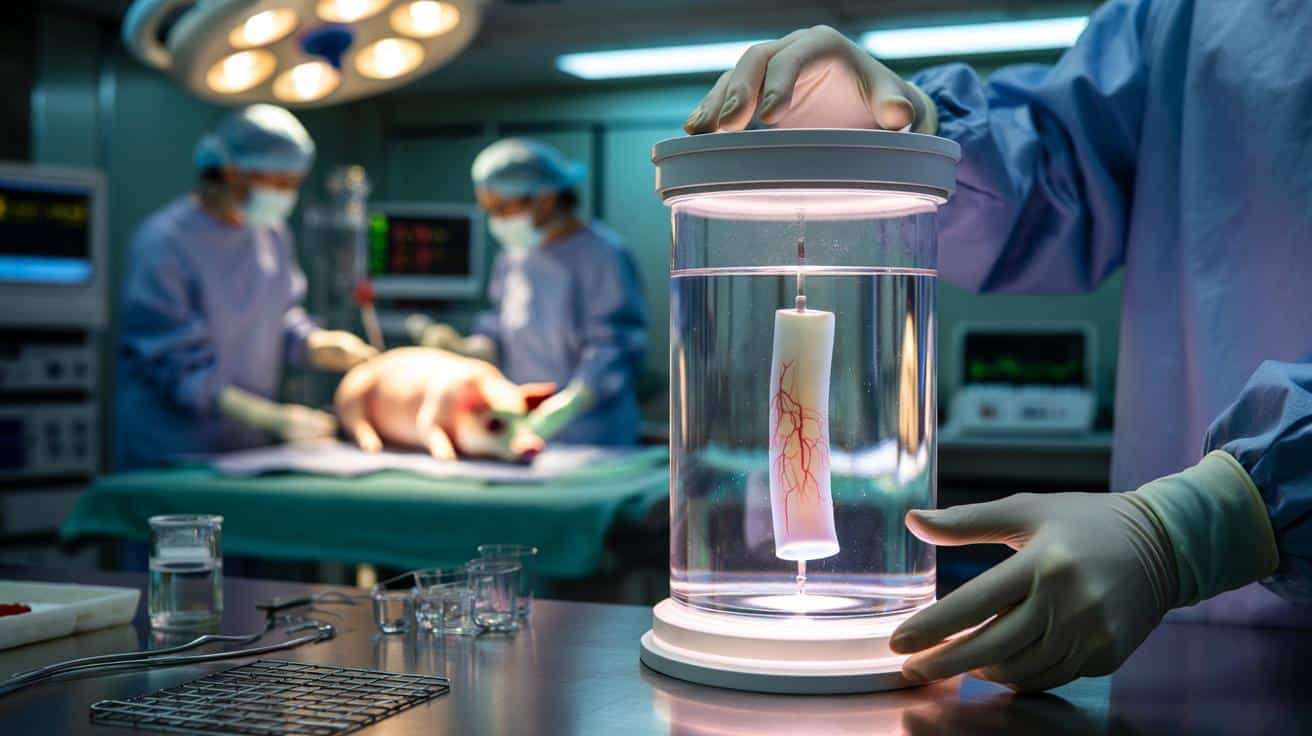
Przełom w medycynie: naukowcy wyhodowali w laboratorium fragment przełyku i skutecznie go przeszczepili
Medycyna regeneracyjna właśnie przekroczyła kolejny próg niemożliwego. Zespół z University College London opracował metodę budowania nowego przełyku z komórek pacjenta osadzonych na zwierzęcym rusztowaniu i z powodzeniem przetestował ją na żywych organizmach. To nie jest teoria z podręcznika – to działająca technologia, która daje realną nadzieję dzieciom rodzącym się bez fragmentu przełyku oraz dorosłym po ciężkich operacjach nowotworowych. Pięć z ośmiu świń z nowym przełykiem przeżyło pół roku i wróciło do normalnego jedzenia.
Najważniejsze informacje:
- Zespół z University College London po raz pierwszy wyhodował przełyk z komórek biorcy na zwierzęcej macierzy
- Osiemmini-świnio-trzymano z nowym przełykiem, pięć przeżyło sześć miesięcy obserwacji
- Przeszczepiony przełyk zaczął funkcjonować jak żywy narząd – kurczył się, przewodził impulsy nerwowe i przesuwał pokarm
- Metoda wykorzystuje inżynierię tkankową – komórki pacjenta na matrycy z przełyku świni
- Cała procedura od pobrania tkanki do gotowego fragmentu trwa około dwóch miesięcy
- Technologia może pomóc dzieciom z długoodcinkową atrezją przełyku
- Metoda może być alternatywą dla pacjentów po operacjach raka przełyku
- Głównym wyzwaniem pozostaje wydłużenie przeszczepianych odcinków do 10-15 cm
To, co jeszcze niedawno wydawało się czystą science fiction, właśnie stało się realnym eksperymentem na żywych organizmach. Zespół z University College London opracował metodę zbudowania „nowego” odcinka przełyku z komórek dawcy i z powodzeniem przetestował go u świń. Taka technika może w przyszłości zmienić sposób leczenia dzieci rodzących się bez fragmentu przełyku oraz dorosłych po ciężkich chorobach nowotworowych.
Mini-świnie z nowym przełykiem: co dokładnie zrobili naukowcy
Badanie przeprowadzono na ośmiu tzw. mini-świniach, ważących około 10 kilogramów. Chirurdzy usunęli każdemu zwierzęciu 2,5-centymetrowy odcinek przełyku. W jego miejsce wszczepiono fragment narządu wyhodowany wcześniej w laboratorium z komórek pochodzących od tych samych osobników.
Osiem świń otrzymało laboratoryjnie skonstruowany fragment przełyku zbudowany na bazie materiału pochodzenia zwierzęcego, uzupełnionego ich własnymi komórkami.
Z opisu pracy opublikowanej w prestiżowym czasopiśmie naukowym wynika, że pięć z tych zwierząt przeżyło okres sześciu miesięcy obserwacji i wróciło do normalnego przyjmowania pokarmu. Kluczowe nie było tylko przeżycie, ale też to, że nowy fragment przełyku zaczął funkcjonować jak żywy, aktywny narząd: kurczył się, przewodził impulsy nerwowe i pozwalał przesuwać pokarm w stronę żołądka.
Jak zbudować „nowy” przełyk z istniejącego narządu
Zespół kierowany przez chirurga dziecięcego Paolo De Coppiego zastosował podejście inżynierii tkankowej. Najpierw pobrano przełyk od świni – służył on jako biologiczny „stelaż”. Następnie z tego narządu usunięto wszystkie komórki, pozostawiając jedynie tzw. macierz zewnątrzkomórkową, czyli rusztowanie z białek, włókien i struktur podtrzymujących.
Taka „pusta” matryca zachowuje dokładny kształt i architekturę przełyku, ale nie zawiera już elementów, które mogłyby wywołać silną reakcję immunologiczną. To właśnie na nią naukowcy nanosili komórki od zwierzęcia, które miało zostać biorcą przeszczepu.
- pobranie przełyku i usunięcie wszystkich komórek
- pozostawienie samej matrycy białkowej narządu
- izolacja komórek mięśniowych od przyszłego biorcy
- przeprogramowanie ich do postaci komórek macierzystych
- zaszczepienie ich na matrycy przełyku
- dojrzewanie w bioraktorze przez około tydzień
Cała procedura, od pierwszego pobrania tkanki do gotowego fragmentu przełyku, trwała około dwóch miesięcy. To czas, który w realnej praktyce klinicznej da się wkomponować w standardową opiekę nad dziećmi z ciężkimi wadami przełyku, gdzie leczenie rozciąga się na tygodnie i miesiące.
Jak sprawdzono, że „sztuczny” przełyk działa
Sam przeszczep to tylko część wyzwania. Badaczy interesowało, czy taki fragment narządu naprawdę połączy się z organizmem, wytworzy naczynia krwionośne, nerwy i mięśnie, i czy przejmie funkcję brakującego odcinka przewodu pokarmowego.
W trakcie operacji każdy implant owinięto biodegradowalną siateczką. Taki „opatrunek” miał pomóc w tworzeniu naczyń krwionośnych, ustabilizować przeszczep i ułatwić jego wrośnięcie w otaczające tkanki. Zgodnie z danymi z Nature Biotechnology wszystkie osiem świń bez komplikacji przeszło najtrudniejszy, pierwszy miesiąc po zabiegu.
Po trzech miesiącach tkanka przeszczepiona świniom była już całkowicie zintegrowana z przełykiem, a pomiary wykazały wystarczające ciśnienie do przesuwania pokarmu do żołądka.
Badacze opisują, że u pięciu zwierząt, które dotrwały do końca półrocznego okresu obserwacji, zaobserwowano:
| Obszar oceny | Efekt po przeszczepie |
|---|---|
| Połykanie | powrót do skutecznego przełykania i normalnego karmienia |
| Mięśnie | powstanie warstwy kurczliwych włókien mięśniowych |
| Nerwy | obecność sieci nerwowej niezbędnej do koordynacji skurczów |
| Naczynia krwionośne | w pełni funkcjonalna sieć naczyń zaopatrujących przeszczep |
U części zwierząt doszło do zwężenia przeszczepionego fragmentu. Zespoły medyczne poradziły sobie z tym, stosując zabiegi endoskopowe, analogiczne do tych, które stosuje się na co dzień u ludzi z podobnym problemem. Trzy świnie uśpiono wcześniej z przyczyn związanych z dobrostanem, a nie bezpośrednio z niewydolnością przeszczepu.
Szansa dla dzieci z ciężkimi wadami przełyku
Jedną z grup, która może najbardziej skorzystać na takiej technologii, są dzieci urodzone z tzw. długoodcinkową atrezją przełyku. W tej rzadkiej wadzie wrodzonej brakuje znacznej części narządu, co uniemożliwia normalne karmienie. Obecnie lekarze próbują radzić sobie z tym na różne sposoby: wyciągają istniejące fragmenty przełyku, używają fragmentu jelita lub żołądka, a cała terapia jest długa i obciążająca dla małego pacjenta.
Przełyk wyhodowany z komórek dziecka i osadzony na zwierzęcej matrycy mógłby rosnąć razem z nim, bez konieczności stosowania agresywnego leczenia immunosupresyjnego.
Zastosowanie tkanki opartej na komórkach własnych pacjenta daje kilka kluczowych korzyści:
- minimalne ryzyko odrzucenia przeszczepu
- brak konieczności przewlekłego osłabiania układu odpornościowego lekami
- możliwość „dopasowania” długości i kształtu fragmentu przełyku do konkretnego dziecka
- szansa, że narząd będzie rósł wraz ze wzrostem organizmu
Dla rodziców dzieci z takimi wadami nawet sama perspektywa terapii, która ogranicza liczbę poważnych operacji i powikłań, ma ogromne znaczenie. To także potencjalna zmiana w codzienności – mniejsza liczba hospitalizacji, łatwiejsze karmienie, lepszy komfort życia.
Droga do zastosowania u ludzi: jakie bariery stoją przed naukowcami
Choć wyniki u świń robią wrażenie, badacze podkreślają, że przed rozpoczęciem prób klinicznych u ludzi trzeba przejść kilka ważnych etapów. Jednym z najtrudniejszych zadań pozostaje wydłużenie przeszczepianych odcinków przełyku do 10–15 centymetrów. To długość, która ma realne znaczenie w ciężkich wadach u dzieci i w sytuacji, gdy u dorosłego usunięto część przełyku z powodu nowotworu.
Przy dłuższych fragmentach najwięcej problemów sprawia doprowadzenie odpowiedniej ilości krwi do całej tkanki. Bez sprawnego, rozgałęzionego układu naczyń krwionośnych komórki w środku takiego przeszczepu zaczynają obumierać, a narząd traci zdolność do pracy. Dlatego zespół pracuje nad ulepszeniem zarówno samej matrycy, jak i sposobu jej „ukrwienia” tuż po wszczepieniu.
Naukowcy próbują też ujednolicić proces produkcji tak, aby zminimalizować ręczną pracę w laboratorium. Chcą przygotowywać zestandaryzowane matryce pochodzenia zwierzęcego, gotowe do „uzupełnienia” komórkami konkretnego pacjenta. To nie tylko kwestia bezpieczeństwa, ale też kosztów i dostępności – jeżeli metoda ma trafić do szpitali, musi być powtarzalna i opłacalna.
Potencjalne zastosowania u dorosłych
Choć w centrum uwagi pozostają dzieci z wadami wrodzonymi, ta technika może przydać się również u dorosłych. Po operacjach raka przełyku chirurdzy często muszą korzystać z fragmentów żołądka lub jelit, co wiąże się z dużymi zabiegami i długą rekonwalescencją. U niektórych pacjentów przełyk zostaje zniszczony przez połknięcie żrącej substancji – na przykład w próbie samobójczej.
Gdyby dało się w takich sytuacjach wstawić fragment przełyku wyhodowany z komórek samego pacjenta, cały zabieg mógłby stać się mniej obciążający dla organizmu. Lekarze mieliby też większą kontrolę nad kształtem i długością przeszczepianej tkanki.
Na czym polega bioraktor i dlaczego jest tak istotny
W opisie badań często przewija się pojęcie bioraktora. W praktyce to specjalne urządzenie, w którym fragment narządu dojrzewa przed wszczepieniem. Bioraktor utrzymuje stałą temperaturę, odpowiednie stężenie tlenu i składników odżywczych w płynie otaczającym tkankę. Często symuluje też delikatne ruchy czy ciśnienie, aby komórki przyzwyczajały się do warunków, które spotkają w ciele.
W przypadku przełyku to szczególnie ważne, bo ten narząd musi znosić bardzo konkretne obciążenia: kontakt z jedzeniem, skurcze mięśni, zmiany ciśnienia. Odpowiednio „wytrenowany” w bioraktorze fragment ma większą szansę, że po wszczepieniu szybko zacznie robić to, czego się od niego oczekuje – czyli przesuwać pokarm w dół.
Co ta technologia mówi o przyszłości medycyny rekonstrukcyjnej
Praca zespołu z Londynu wpisuje się w szerszy trend w medycynie: od odtwarzania kształtu narządów w kierunku przywracania ich pełnej funkcji. Do niedawna w wielu przypadkach lekarze mogli zaoferować pacjentom jedynie rozwiązania zastępcze, jak plastikowe protezy czy „łatki” z innej tkanki. Coraz częściej pojawiają się metody, które próbują budować narządy od wewnątrz, na poziomie komórek.
Takie podejście niesie ze sobą zarówno szanse, jak i ryzyka. Z jednej strony umożliwia projektowanie tkanek niemal „na zamówienie”, dopasowanych do konkretnego pacjenta. Z drugiej – każdy kolejny krok wymaga bardzo uważnych testów bezpieczeństwa. Nie chodzi tylko o skuteczność samego przeszczepu, lecz także o długofalowe konsekwencje, w tym ryzyko niekontrolowanego wzrostu komórek czy powstania nieprawidłowych struktur.
Dla pacjentów i lekarzy najbliższe lata będą więc okresem rosnących oczekiwań, ale też konieczności chłodnej oceny nowych terapii. Jeżeli kolejne badania na zwierzętach potwierdzą bezpieczeństwo i powtarzalność opisanej metody, pierwsze próby kliniczne u ludzi mogą rozpocząć się w ciągu kilku lat. Stawka jest wysoka: możliwość przywrócenia normalnego jedzenia dzieciom i dorosłym, którzy dziś często spędzają sporą część życia w szpitalach, walcząc o coś tak podstawowego, jak przełknięcie kęsa.
Najczęściej zadawane pytania
Czy ta metoda jest już dostępna dla ludzi?
Nie, badania prowadzono dotych tylko na świniach. Przed próbami klinicznymi u ludzi naukowcy muszą wydłużyć przeszczepiane odcinki i potwierdzić bezpieczeństwo.
Jak zbudowano przełyk w laboratorium?
Naukowcy użyli przełyku świni jako matrycy, usunęli komórki, a na puste rusztowanie nanieśli komórki mięśniowe pobrane od biorcy. Następnie fragment dojrzewał w bioraktorze przez około tydzień.
Komu może pomóc ta technologia?
Przede wszystkim dzieciom z długoodcinkową atrezją przełyku (wada wrodzona) oraz dorosłym po operacjach usunięcia przełyku z powodu nowotworu lub połknięcia substancji żrącej.
Jakie są główne zalety przeszczepu z komórek pacjenta?
Minimalne ryzyko odrzucenia przeszczepu, brak konieczności przewlekłego stosowania leków immunosupresyjnych, możliwość dopasowania kształtu do konkretnego pacjenta, szansa że narząd będzie rósł wraz z organizmem.
Kiedy mogą rozpocząć się badania na ludziach?
Jeśli kolejne badania na zwierzętach potwierdzą bezpieczeństwo i powtarzalność metody, pierwsze próby kliniczne u ludzi mogą rozpocząć się w ciągu kilku lat.
Wnioski
Choć do pierwszych prób klinicznych u ludzi miną jeszcze lata, ten przełom zmienia fundamentalne podejście do medycyny rekonstrukcyjnej. Zamiast zastępować narządy protezami, naukowcy uczą się je odbudowywać od poziomu komórek. Dla pacjentów z atrezją przełyku lub po operacjach raka to realna perspektywa normalnego życia bez wieloletnich hospitalizacji i agresywnego leczenia immunosupresyjnego. Warto śledzić postępy badań – jeśli potwierdzi się bezpieczeństwo metody, może się ona stać standardem w ciągu najbliższej dekady.
Podsumowanie
Naukowcy z University College London po raz pierwszy wyhodowali fragment przełyku w laboratorium i pomyślnie przeszczepili go ośmiu mini-świnom. Pięć zwierząt przeżyło sześć miesięcy i wróciło do normalnego przyjmowania pokarmu. To przełomowe osiągnięcie może w przyszłości pomóc dzieciom urodzonym bez fragmentu przełyku oraz dorosłym po operacjach nowotworowych.