Przełom w medycynie: hodowla i udana przeszczep oskrzeli przełyku u świń
Stoimy na progu medycznej rewolucji, w której brakujące części ciała będziemy hodować w laboratoriach zamiast zastępować je sztywnymi protezami. Brytyjscy specjaliści właśnie udowodnili, że stworzenie funkcjonalnego fragmentu przełyku z własnych komórek pacjenta jest nie tylko możliwe, ale i wysoce skuteczne. To przełomowe osiągnięcie sprawia, że scenariusze z filmów science fiction stają się realną nadzieją dla dzieci i dorosłych z ciężkimi uszkodzeniami przewodu pokarmowego.
Najważniejsze informacje:
- Zespół z University College London wyhodował funkcjonalny fragment przełyku przy użyciu macierzy pozakomórkowej i komórek biorcy.
- Przeszczepione fragmenty u świń wytworzyły własne mięśnie, nerwy oraz naczynia krwionośne, umożliwiając normalne połykanie.
- Nowa metoda eliminuje konieczność stosowania leków przeciw odrzuceniu przeszczepu, ponieważ tkanka powstaje z komórek pacjenta.
- Technologia daje nadzieję na skuteczne leczenie noworodków z długoodcinkową atrezją przełyku oraz dorosłych po leczeniu nowotworów.
- Głównym wyzwaniem przed badaniami na ludziach jest zwiększenie długości przeszczepu do 10–15 cm i zapewnienie mu odpowiedniego unaczynienia.
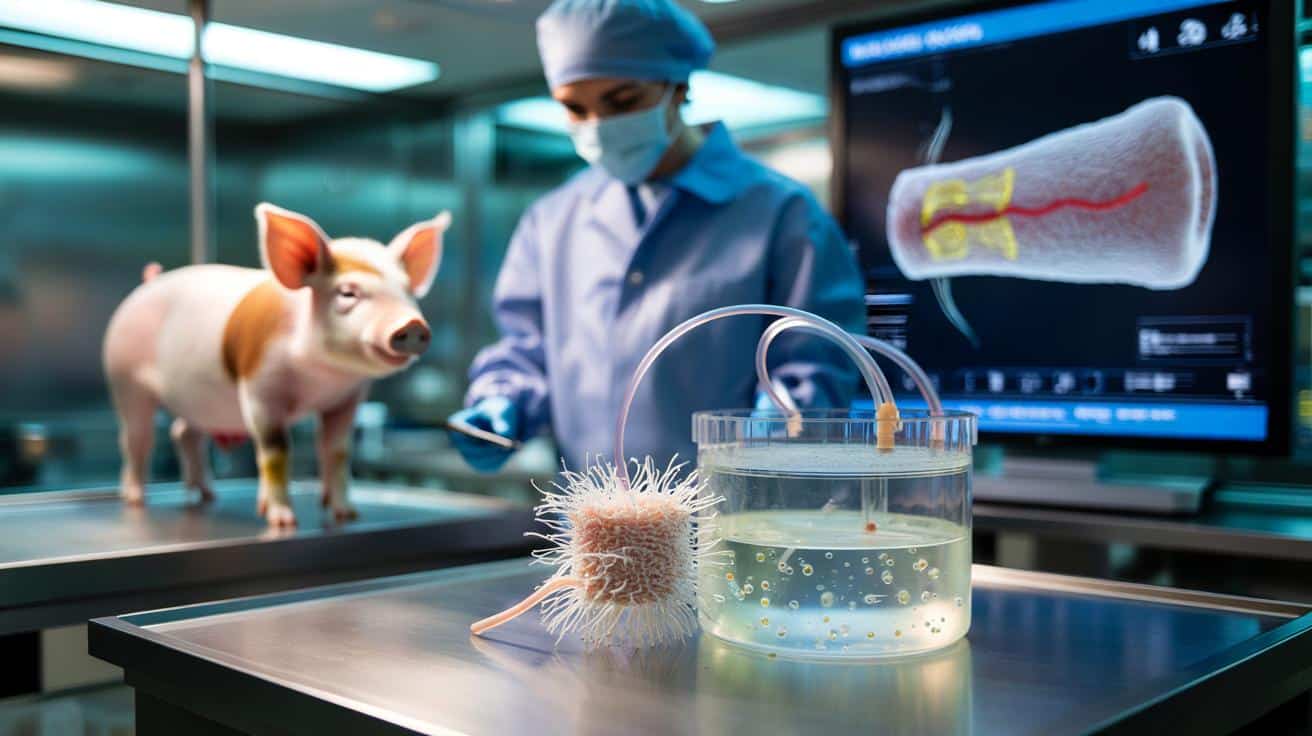
Brytyjscy naukowcy po raz pierwszy wyhodowali w laboratorium fragment przełyku z komórek świń i pomyślnie go przeszczepili.
To, co jeszcze niedawno brzmiało jak scenariusz filmu science fiction, właśnie stało się realnym eksperymentem. Miniaturowe świnie odzyskały normalne jedzenie po tym, jak wszczepiono im fragment przełyku skonstruowany z ich własnych komórek. Badacze widzą w tym szansę dla dzieci rodzących się z ciężkimi wadami przewodu pokarmowego, ale także dla dorosłych po nowotworach lub urazach chemicznych.
Dlaczego przełyk jest tak trudny do naprawy
Przełyk nie jest zwykłą rurą, którą można zastąpić dowolną protezą. To narząd, który:
- musi wykonywać precyzyjne skurcze mięśni, aby przesuwać kęs do żołądka,
- przekazuje sygnały nerwowe koordynujące te skurcze,
- znosi stałe obciążenia mechaniczne i kontakt z jedzeniem oraz płynami,
- powinien rosnąć razem z organizmem dziecka.
Dlatego klasyczne metody rekonstrukcji – na przykład wykorzystanie fragmentu jelita lub żołądka – są trudne technicznie i obarczone licznymi powikłaniami. Chirurdzy dziecięcy szczególnie zmagają się z tzw. długoodcinkową atrezją przełyku, gdy znaczna część przewodu po prostu się nie wykształciła.
Naukowcy postanowili nie tylko „zszyć brakujący odcinek”, ale stworzyć żywą tkankę, która zachowuje się jak naturalny przełyk i może rozwijać się razem ze zwierzęciem.
Jak stworzono biologiczny „szkielet” z tkanki zwierzęcej
Zespół z University College London, kierowany przez chirurga dziecięcego Paolo De Coppiego, wykorzystał narzędzia inżynierii tkankowej. Najpierw pobrano przełyk od świni. Następnie usunięto z niego wszystkie żywe komórki, pozostawiając jedynie tzw. macierz pozakomórkową – naturalny, białkowy ruszt.
Taka „pusta” struktura:
- zachowuje kształt i układ włókien oryginalnego narządu,
- pozbawiona jest elementów najbardziej odpowiedzialnych za odrzucenie przeszczepu,
- może zostać zasiedlona nowymi komórkami pochodzącymi od przyszłego biorcy.
Do przygotowanego rusztu wprowadzono komórki mięśniowe pobrane od samych mini-świń, które miały otrzymać przeszczep. Komórki te przeprogramowano do formy bardziej „plastycznej” – przypominającej komórki macierzyste, zdolne do tworzenia różnych typów tkanek. Następnie umieszczono je w bioraktorze, czyli specjalnym urządzeniu imitującym warunki panujące w organizmie.
Przez tydzień w bioraktorze komórki miały czas, by przyczepić się do rusztu i zacząć organizować się w warstwę przypominającą naturalny przełyk. Cały proces przygotowania jednego implantu trwał około dwóch miesięcy, co – jak podkreślają badacze – da się pogodzić z planowaniem leczenia dzieci z ciężką wadą przełyku.
Eksperyment na mini-świniach: co udało się osiągnąć
Usunięty fragment i laboratoryjny „zamiennik”
Do badania wybrano osiem miniaturowych świń, ważących około 10 kilogramów. Chirurdzy wycięli każdemu zwierzęciu niewielki, 2,5-centymetrowy fragment przełyku. W jego miejsce wszyto laboratoryjnie przygotowaną tkankę opartą na zwierzęcej macierzy i komórkach samego biorcy.
Nowy odcinek przełyku otoczono dodatkowo biodegradowalną siatką. Miała ona spełnić dwie funkcje: wzmocnić mechanicznie świeży przeszczep i pobudzić tworzenie się nowych naczyń krwionośnych.
Kluczowe pytanie brzmiało: czy tak zrekonstruowany fragment włączy się w pracę całego przewodu pokarmowego, wytrzyma codzienną dietę i będzie rósł razem ze zwierzęciem.
Co pokazało pół roku obserwacji
Badanie opisane w prestiżowym czasopiśmie biotechnologicznym przyniosło obiecujące wyniki. Wszystkie osiem świń przeszło bez powikłań najbardziej ryzykowny okres pierwszych 30 dni po operacji. W tym czasie najczęściej dochodzi do nieszczelności, zakażeń czy gwałtownego odrzucenia przeszczepu.
Pięć zwierząt przeżyło pełne sześć miesięcy obserwacji. U nich odtworzony fragment przełyku:
- wytworzył czynne mięśnie zdolne do kurczenia,
- rozwinął sieć nerwów przewodzących impulsy sterujące ruchem,
- uzyskał działające naczynia krwionośne, zapewniające stały dopływ tlenu i składników odżywczych,
- wytwarzał odpowiednie ciśnienie potrzebne do przesuwania pokarmu do żołądka.
Z punktu widzenia zwierząt najważniejszy efekt był prosty: odzyskały naturalne połykanie pokarmu. Jedzenie przechodziło z jamy ustnej do żołądka bez większych zaburzeń.
Trzy pozostałe świnie uśpiono wcześniej z powodów dobrostanu – nie z powodu nagłego niepowodzenia samego przeszczepu, ale z uwagi na sumę komplikacji i wymogi etyczne obowiązujące w takich badaniach.
Zwężenia i jak sobie z nimi poradzono
U części zwierząt doszło do zwężenia odtworzonego fragmentu przełyku. To dość typowe powikłanie także u ludzi po podobnych operacjach. Zastosowano więc zabiegi endoskopowe, bardzo zbliżone do tych, które wykonują gastroenterolodzy u pacjentów – poszerzano przełyk od środka za pomocą specjalnych narzędzi wprowadzonych przez jamę ustną.
Takie postępowanie okazało się skuteczne i pokazało, że zrekonstruowana tkanka reaguje na terapię w sposób zbliżony do naturalnego narządu.
Od świń do ludzi: co jeszcze trzeba dopracować
Największa bariera: unaczynienie i długość przeszczepu
Naukowcy nie ukrywają, że przed pierwszymi zabiegami u ludzi czeka ich jeszcze kilka kluczowych wyzwań. Obecnie testowany fragment miał zaledwie 2,5 cm. U dzieci z ciężką atrezją czy u dorosłych po rozległym usunięciu przełyku potrzebne są o wiele dłuższe odcinki – nawet 10–15 cm.
| Parametr | Obecny etap badań | Cel dla zastosowań klinicznych |
|---|---|---|
| Długość fragmentu przełyku | ok. 2,5 cm | 10–15 cm |
| Czas hodowli w laboratorium | ok. 2 miesiące | utrzymanie lub skrócenie przy zachowaniu jakości |
| Zakres badań | 8 mini-świń | szersze badania przedkliniczne i testy bezpieczeństwa |
Im dłuższy przeszczep, tym większy problem z zapewnieniem równomiernego dopływu krwi. Bez dobrze rozbudowanej sieci naczyń tkanka w środkowych odcinkach narządu zaczyna obumierać. To może prowadzić do nieszczelności i groźnych zakażeń. Dlatego część zespołu pracuje obecnie nad ulepszeniem sposobów „przekrwienia” dłuższych konstrukcji jeszcze przed ich wszczepieniem.
Standaryzacja i personalizacja jednocześnie
Badacze chcą doprowadzić do sytuacji, w której w banku tkanek dostępne będą gotowe macierze przełyku pochodzenia zwierzęcego – dokładnie oczyszczone, przebadane i opisane. Personalizacja następowałaby dopiero na etapie zasiedlania ich komórkami konkretnego pacjenta.
Taki model niesie dwie wyraźne korzyści: eliminuje konieczność długotrwałego stosowania silnych leków przeciw odrzuceniu oraz daje szansę na implant, który będzie rósł razem z dzieckiem. To szczególnie istotne w chirurgii pediatrycznej, gdzie każdy „sztywny” element może po kilku latach stać się za mały.
Kto może w przyszłości skorzystać z tej technologii
Szef zespołu badawczego ocenia, że przy sprzyjających wynikach dalszych testów pierwsze badania kliniczne z udziałem ludzi mogą ruszyć za 3–4 lata. Na liście potencjalnych beneficjentów są przede wszystkim:
- noworodki z długoodcinkową atrezją przełyku,
- dzieci z innymi złożonymi wadami w obrębie górnego odcinka przewodu pokarmowego,
- dorośli po radykalnym leczeniu raka przełyku,
- osoby, u których kwasy żrące trwale zniszczyły fragment przełyku.
Obecne metody rekonstrukcji często oznaczają wielogodzinne operacje, liczne powikłania i długą rehabilitację. Bioinżynieryjny przeszczep mógłby w części przypadków skrócić czas leczenia i zredukować liczbę zabiegów, choć sam w sobie pozostaje skomplikowaną procedurą chirurgiczną.
Szerszy obraz: medycyna regeneracyjna w praktyce
Eksperyment z przełykiem wpisuje się w szerszy trend medycyny regeneracyjnej. Zbliżone podejścia testuje się już przy odtwarzaniu fragmentów tchawicy, pęcherza moczowego czy naczyń krwionośnych. W każdym z tych przypadków naukowcy łączą naturalny ruszt białkowy z komórkami własnymi pacjenta.
Takie hybrydowe konstrukcje różnią się od klasycznych protez z tworzyw sztucznych. Nie są jednorazowym „wkładanym elementem”, tylko żywą tkanką, która może reagować na bodźce, goić się, a w pewnym stopniu nawet przebudowywać. Daje to szansę na bardziej naturalne funkcjonowanie narządów i mniejszą liczbę długoterminowych komplikacji.
Dla rodziców dzieci z ciężkimi wadami przewodu pokarmowego tego typu badania mogą oznaczać realną zmianę rokowania w perspektywie kilku lat. Z kolei lekarze liczą na poszerzenie arsenału metod rekonstrukcyjnych w przypadkach, gdzie obecnie możliwości są mocno ograniczone.
W tle pozostają pytania o koszty, dostępność i przygotowanie zespołów chirurgicznych do tak zaawansowanych procedur. Do tego dochodzi potrzeba bardzo dokładnego monitorowania pacjentów przez lata, aby wychwycić ewentualne niepożądane zmiany w przebudowującej się tkance. Jeżeli jednak kolejne badania potwierdzą bezpieczeństwo i efektywność tej metody, przełyk z laboratorium może stać się jednym z bardziej namacalnych przykładów tego, jak inżynieria tkankowa przechodzi z etapu eksperymentów do codziennej praktyki klinicznej.
Najczęściej zadawane pytania
Na czym polegał innowacyjny eksperyment z przełykiem?
Naukowcy pobrali przełyk od świni, usunęli z niego komórki, pozostawiając jedynie białkowy ruszt, który następnie zasiedlili przeprogramowanymi komórkami biorcy i wyhodowali w bioreaktorze.
Jakie są najważniejsze zalety wyhodowanego w laboratorium przełyku?
Taki implant jest żywą tkanką, która rośnie wraz z organizmem, posiada własne unaczynienie i układ nerwowy, a także nie jest odrzucana przez układ odpornościowy pacjenta.
Kto będzie mógł skorzystać z tej technologii w przyszłości?
Potencjalnymi beneficjentami są noworodki z ciężkimi wadami przewodu pokarmowego, dorośli po leczeniu raka przełyku oraz osoby po oparzeniach chemicznych przełyku.
Kiedy możemy spodziewać się pierwszych operacji u ludzi?
Przy pomyślnym przebiegu dalszych testów bezpieczeństwa, pierwsze badania kliniczne z udziałem pacjentów mogą rozpocząć się za około 3 do 4 lat.
Wnioski
Sukces eksperymentu na zwierzętach to kamień milowy w rozwoju medycyny regeneracyjnej, który za kilka lat może trwale zmienić standardy chirurgii rekonstrukcyjnej. Choć przed naukowcami jeszcze wyzwania związane z unaczynieniem dłuższych odcinków tkanki, kierunek zmian jest jasny: przyszłość należy do personalizowanych, żywych implantów. Dla pacjentów oznacza to mniej powikłań, krótszą rehabilitację i powrót do naturalnego funkcjonowania organizmu.
Podsumowanie
Brytyjscy naukowcy z powodzeniem przeszczepili miniaturowym świniom fragmenty przełyku wyhodowane w laboratorium z ich własnych komórek. Ten sukces inżynierii tkankowej otwiera drogę do rewolucyjnych metod leczenia dzieci z wadami wrodzonymi oraz dorosłych po operacjach onkologicznych.