Przełom w leczeniu raka głowy i szyi związanego z HPV. Nowy cel dla immunoterapii
Rak głowy i szyi wywołany wirusem HPV coraz częściej dotyczy młodszych, niepalących osób, a spora część guzów nie reaguje na dostępne terapie.
Nowe badania zespołu z Henry Ford Health i Michigan State University pokazują, że kluczem do opanowania tych szczególnie opornych nowotworów może być jedna, ściśle określona cząsteczka. Jej zablokowanie sprawia, że guz przestaje się kamuflować przed układem odpornościowym i zaczyna być podatny na działanie immunoterapii.
Rak głowy i szyi związany z HPV – cichy wzrost zachorowań
W onkologii laryngologicznej coraz większą część przypadków stanowią nowotwory jamy ustnej i gardła wywołane zakażeniem wirusem brodawczaka ludzkiego, czyli HPV. W Stanach Zjednoczonych liczba takich rozpoznań osiąga poziom, który lekarze określają już mianem sytuacji przypominającej falę epidemiczną.
Wcześniej nowotwory tej okolicy kojarzono głównie z paleniem papierosów i alkoholem. Nowa grupa pacjentów to często osoby w średnim wieku, bez obciążeń w postaci nałogów. Dla wielu z nich standardowe leczenie – operacje, radioterapia, chemioterapia, a nawet nowoczesna immunoterapia – okazuje się niewystarczające.
Przeczytaj również: Ból pleców a rak jelita grubego? Lekarz wyjaśnia, kiedy się bać
Dlaczego część guzów jest praktycznie niewidoczna dla odporności
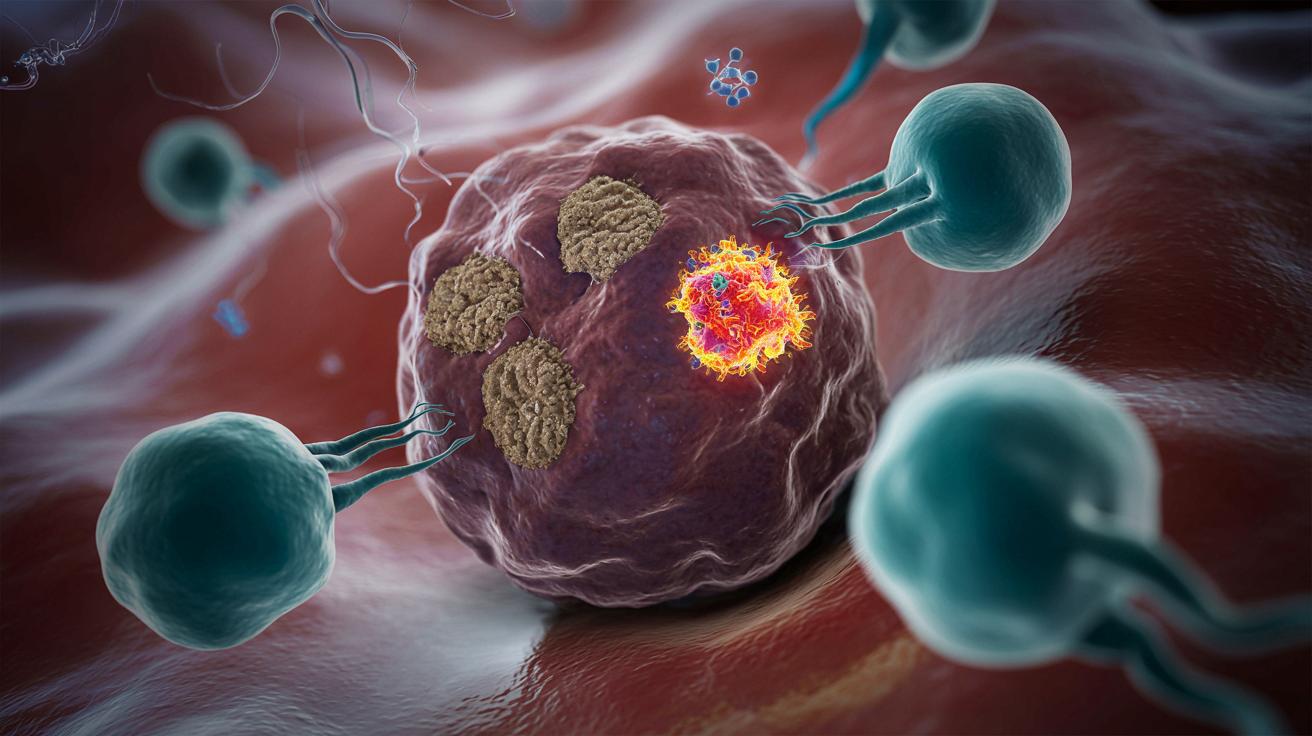
Układ odpornościowy rozpoznaje chore komórki dzięki specjalnym cząsteczkom na ich powierzchni. To tzw. kompleks zgodności tkankowej klasy I (MHC-I). Działają jak molekularne „tablice rejestracyjne”, na których komórka pokazuje fragmenty tego, co dzieje się w jej wnętrzu.
W przypadku raka głowy i szyi powiązanego z HPV wiele guzów prawie całkowicie traci te cząsteczki. W efekcie limfocyty T CD8+ i komórki NK, które normalnie patrolują organizm i usuwają podejrzane komórki, przechodzą obok guza, jakby nic się nie działo.
Przeczytaj również: Ten prosty ruch z Pilates odmładza ciało po 50. roku życia
Bez MHC-I na powierzchni komórki rakowe stają się dla odporności czymś w rodzaju niewidzialnego intruza. Leków immunokompetentnych nie ma do czego „nakierować”.
Leki z grupy inhibitorów punktów kontrolnych, jak przeciwciała anty-PD-1, potrafią wybudzić limfocyty T z uśpienia. Jeżeli jednak te limfocyty nie widzą celu, cała terapia traci sens. Do tej pory badacze nie mieli pełnego obrazu, dlaczego właśnie guzy związane z HPV tak skutecznie gubią swoje molekularne „sygnały alarmowe”.
MARCHF8 – białko, które pomaga rakowi się ukryć
W pracy opublikowanej w piśmie „Proceedings of the National Academy of Sciences” międzynarodowy zespół kierowany przez mikrobiologa i immunologa Dohuna Pyeona wskazuje winowajcę: białko MARCHF8.
Przeczytaj również: Jak okolica, w której mieszkasz, może zmniejszyć ryzyko udaru mózgu
Wirus HPV przejmuje kontrolę nad tą cząsteczką i wykorzystuje ją przeciwko gospodarzowi. MARCHF8 odpowiada za regulowanie ilości różnych białek na powierzchni komórki. Pod wpływem HPV zostaje tak „przeprogramowane”, by usuwać z błony komórkowej właśnie MHC-I.
Efekt jest dramatyczny: powierzchnia komórki nowotworowej praktycznie pustoszeje z sygnałów, które mogłyby przyciągnąć limfocyty T. Guz nabiera cech tzw. „zimnego” nowotworu – słabo nacieczonego przez komórki odpornościowe, odpornego na większość strategii immunoterapeutycznych.
Co się dzieje, gdy wyłączymy MARCHF8
Badacze poszli o krok dalej i za pomocą metod genetycznych usunęli MARCHF8 w modelu myszy z opornymi guzami związanymi z HPV. Nagle „niewidzialne” komórki rakowe zaczęły znowu prezentować MHC-I na swojej powierzchni.
Po wyciszeniu MARCHF8 system odpornościowy myszy rozpoczął intensywny atak na guzy, które wcześniej pozostawały praktycznie nienaruszone mimo terapii.
W wielu przypadkach wzrost nowotworu wyraźnie zwolnił, a u części zwierząt nie wykryto już rozwiniętej zmiany. To sugeruje, że sam powrót MHC-I wystarcza, aby przywrócić zdolność organizmu do rozpoznawania i eliminowania komórek rakowych.
Jak zmienia się mikrośrodowisko guza po zablokowaniu MARCHF8
Badacze dokładnie przeanalizowali, co dzieje się w otoczeniu guza po manipulacji MARCHF8. Okazało się, że obraz mikroskopowy nowotworu zmienia się bardzo wyraźnie.
- Do guza napływa wiele limfocytów T CD8+, czyli „żołnierzy pierwszej linii” odpowiedzialnych za niszczenie komórek rakowych.
- Zwiększa się liczba komórek NK, które atakują komórki pozbawione prawidłowych sygnałów zgodności tkankowej.
- Wzrasta obecność makrofagów, które przejmują rolę „sprzątaczy” i regulatorów stanu zapalnego.
- Spada udział komórek o działaniu tłumiącym odpowiedź odpornościową.
Mohamed Khalil, współautor pracy, opisuje ten proces jako silne pobudzenie i napływ aktywnych komórek odpornościowych w rejon guza. To właśnie z takiego obrazu bierze się podział na nowotwory „zimne” i „gorące”. Te drugie są dużo bardziej podatne na działanie immunoterapii, bo mają bogaty „krajobraz” komórek odpornościowych w swoim sąsiedztwie.
Połączenie z immunoterapią anty-PD-1 – obiecujące wyniki u myszy
Najciekawsze efekty pojawiły się, gdy zespół połączył wyciszenie MARCHF8 z terapią anty-PD-1. W modelu myszy z rakiem opornym na samo anty-PD-1, dodanie blokady MARCHF8 wyraźnie zmieniło obraz choroby.
U trzech na dziewięć myszy uzyskano stan pełnej remisji, czyli brak widocznego guza. U pozostałych zwierząt rozwój nowotworu istotnie zahamował. Analizy immunologiczne pokazały gwałtowny wzrost aktywności cytotoksycznej limfocytów T CD8+ i komórek NK, co potwierdza, że mechanizm ataku został skutecznie uruchomiony.
Połączenie blokady MARCHF8 z anty-PD-1 sprawia, że guz z obojętnego immunologicznie staje się intensywnie nacieczony i podatny na uderzenie ze strony limfocytów.
Według kierującego programem immunologii w Instytucie Raka Henry’ego Forda Qing-Shenga Mi, te obserwacje pokazują nie tylko, że podejście działa, ale także ujawniają dokładny sposób, w jaki udaje się „przeprogramować” komunikację między układem odpornościowym a nowotworem.
Co to może oznaczać dla przyszłych pacjentów
Kolejny krok dla zespołu jest dość jasno zarysowany: trzeba opracować lek, który zablokuje MARCHF8 w komórkach ludzkich. Idealnie – taki, który można będzie łączyć z istniejącymi już terapiami immunologicznymi.
Potencjalny preparat nie musiałby sam w sobie niszczyć guza. Jego zadaniem byłoby przywrócenie zdolności układu odpornościowego do rozpoznawania wroga, co otworzy drogę dla obecnych już leków, takich jak przeciwciała anty-PD-1 czy inne inhibitory punktów kontrolnych.
| Element terapii | Rola w leczeniu raka HPV+ |
|---|---|
| Blokada MARCHF8 | Przywraca MHC-I na powierzchni komórek nowotworowych, usuwa „płaszczyk niewidzialności”. |
| Immunoterapia anty-PD-1 | Aktywuje limfocyty T, które znów widzą cel i mogą go zaatakować. |
| Komórki NK i makrofagi | Wspierają limfocyty T w niszczeniu guza i porządkowaniu ogniska zapalnego. |
Adresatami takiej terapii mogliby być przede wszystkim pacjenci, u których standardowe metody zawiodły. Chodzi o osoby z guzami HPV-zależnymi, które nie reagują na radioterapię, klasyczną chemioterapię ani na same inhibitory PD-1.
HPV, szczepienia i profilaktyka – szerszy kontekst badań
Choć opisywane prace skupiają się na leczeniu zaawansowanego raka, trudno pominąć szerszy kontekst związany z profilaktyką zakażeń HPV. Ten wirus odpowiada nie tylko za raka szyjki macicy, ale również za część nowotworów odbytu, prącia oraz głowy i szyi.
W Polsce wciąż trwa proces rozszerzania programu szczepień przeciw HPV. Dla młodzieży, zarówno dziewcząt, jak i chłopców, takie szczepienie może znacząco zmniejszyć ryzyko rozwoju nowotworów w dorosłym życiu. Dla osób już zakażonych szczepionka nie leczy istniejącej choroby, ale ograniczenie krążenia wirusa w populacji z czasem zmniejsza liczbę nowych przypadków raka.
Równolegle rośnie znaczenie regularnych kontroli stomatologicznych i laryngologicznych. Długotrwałe chrypki, problemy z przełykaniem, guzki na szyi czy zmiany w jamie ustnej, które nie goją się przez kilka tygodni, wymagają pilnej konsultacji. Wcześnie wykryty rak głowy i szyi daje znacznie większe szanse na wyleczenie i mniej okaleczające leczenie.
Na co zwracać uwagę w nadchodzących latach
Jeżeli prace nad inhibitorami MARCHF8 wejdą w fazę badań klinicznych, możemy oczekiwać nowych kombinacji leków dla pacjentów onkologicznych. Najpewniej będą to terapie skojarzone, w których blokada MARCHF8 stanie się jednym z elementów większej układanki – obok immunoterapii, radioterapii czy zabiegów chirurgicznych.
W praktyce dla chorych i lekarzy ważne będzie kilka kwestii: jak bezpiecznie blokować MARCHF8, aby nie zaburzyć funkcjonowania zdrowych tkanek; jak dobrać grupę pacjentów, którzy najbardziej skorzystają z takiej terapii; oraz jak monitorować odpowiedź immunologiczną tak, aby zmaksymalizować skuteczność, a ograniczyć działania niepożądane.
Sam pomysł „ściągania płaszcza niewidzialności” z guza wpisuje się w rosnący trend w onkologii, gdzie zamiast wyłącznie niszczyć komórki nowotworowe coraz częściej stawia się na uruchomienie precyzyjnego, własnego systemu obronnego organizmu. Jeżeli uda się bezpiecznie przekuć te wyniki z modeli zwierzęcych na terapię ludzi, pacjenci z rakiem głowy i szyi związanym z HPV mogą zyskać realną, nową szansę na skuteczne leczenie w sytuacjach, które dziś wydają się bez wyjścia.