Nowa broń w walce z rakiem prostaty: immunologiczne „haczyki” na komórki nowotworowe
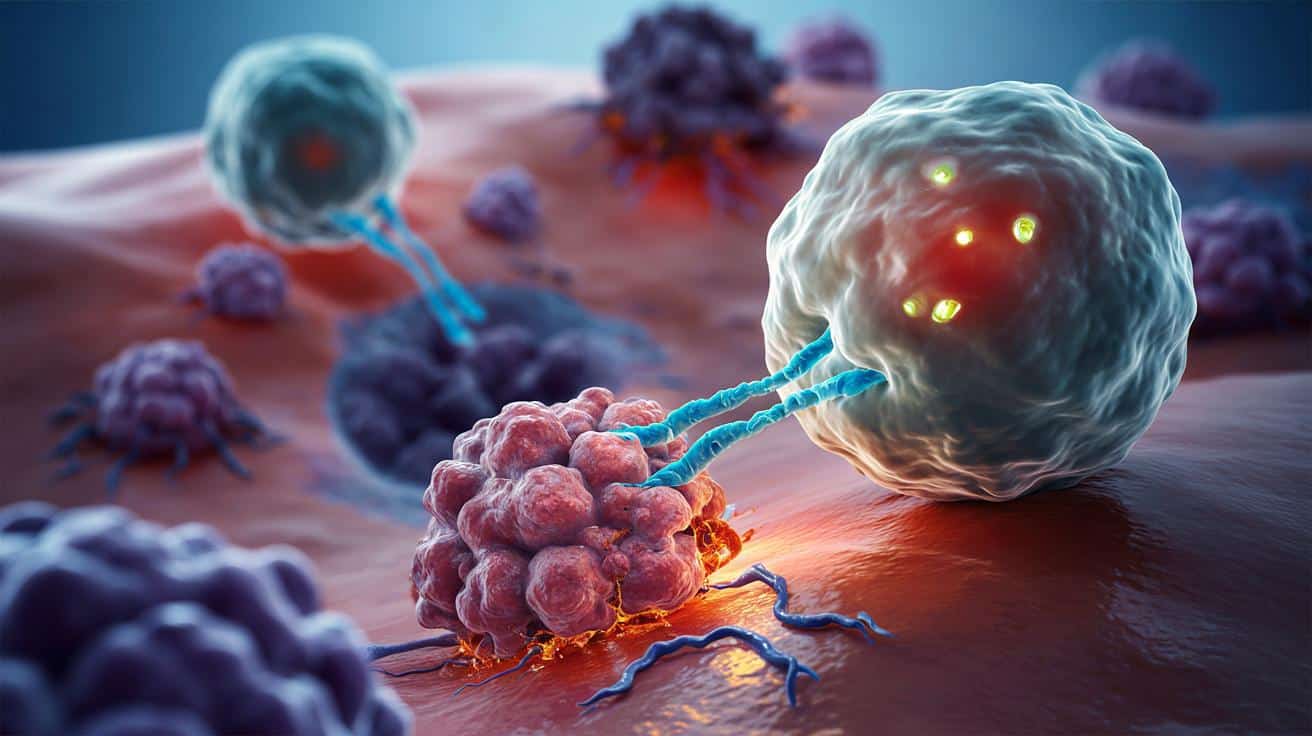
Amerykańscy naukowcy zaprojektowali limfocyty T tak, by dosłownie „zahaczały się” o guz prostaty i nie puszczały, aż zniszczą komórki raka.
To nie kolejna ogólna koncepcja, lecz precyzyjna modyfikacja na poziomie jednego aminokwasu w receptorze komórki odpornościowej. Tak drobna zmiana sprawiła, że limfocyty T zaczęły znacznie skuteczniej przywierać do komórek nowotworu prostaty, blokując jego wzrost u zwierząt laboratoryjnych. Badacze z UCLA, Stanford i kilku innych amerykańskich ośrodków liczą, że ta metoda stanie się zalążkiem nowej generacji terapii dla tzw. guzów litych.
Dlaczego układ odpornościowy tak słabo radzi sobie z rakiem prostaty
Immunoterapia w raku prostaty od lat rozczarowuje. W teorii sprawa wydaje się prosta: limfocyty T rozpoznają na powierzchni komórek nowotworowych charakterystyczne białka i powinny je eliminować. W tym przypadku głównym celem jest PAP, czyli fosfataza kwaśna sterczowa, obecna na ogromnej większości guzów prostaty.
W praktyce organizm gra bardzo zachowawczo. W procesie dojrzewania limfocytów T usuwane są te najsilniejsze i najbardziej agresywne, żeby nie atakowały zdrowych tkanek. Skutek uboczny: pozostają komórki odpornościowe o mocno osłabionych receptorach. Owszem, potrafią rozpoznać PAP, ale wiążą się z komórką nowotworową krótko i zbyt słabo, by ją skutecznie zabić.
Przeczytaj również: Jak okolica, w której mieszkasz, może zmniejszyć ryzyko udaru mózgu
W efekcie limfocyt podchodzi do guza, dotyka go, „widzi”, że coś jest nie tak, po czym po chwili się odkleja. Rak nadal rośnie, a immunoterapia, która w innych nowotworach robi ogromną różnicę, w przypadku prostaty często daje tylko umiarkowane korzyści.
Kluczowy problem w raku prostaty nie leży tylko w rozpoznaniu guza przez komórki odpornościowe, lecz w utrzymaniu mocnego, trwałego kontaktu z komórką nowotworową.
Jak działa technika „catch bond engineering” – czyli inżynieria haczyków
Zespół z UCLA i Stanford postanowił nie wzmacniać całego układu odpornościowego, lecz skupić się na samym „uchwycie”, którym limfocyt T trzyma komórkę raka. Receptor TCR na powierzchni limfocytu to skomplikowana cząsteczka białkowa, zbudowana między innymi z szeregu aminokwasów. Naukowcy zidentyfikowali konkretny receptor (oznaczony jako TCR156), a następnie zmienili w nim tylko jeden aminokwas.
Przeczytaj również: Włoski na brodzie u kobiet: kiedy to norma, a kiedy sygnał alarmowy
Zastosowana metoda nosi nazwę „catch bond engineering”. W praktyce chodzi o to, by połączenie między limfocytem a komórką nowotworową zachowywało się jak haczyk: im większe napięcie mechaniczne, tym mocniej trzyma. W naturalnych warunkach typowe wiązanie białko–białko łatwo pęka pod obciążeniem. Tu działa odwrotna zasada – gdy limfocyt zaczyna „ciągnąć” komórkę raka, więź się wzmacnia.
Po zmianie jednego lub dwóch aminokwasów receptor nie zmienił ogólnego kształtu, więc nadal rozpoznaje wyłącznie właściwy cel. Zmieniła się za to jego mechanika. Limfocyt T przestaje być delikatnym obserwatorem, a staje się myśliwym, który wczepia się w komórkę nowotworową i nie rezygnuje po krótkiej próbie.
Przeczytaj również: Ból pleców a rak jelita grubego? Lekarz wyjaśnia, kiedy się bać
Co zyskuje tak zmodyfikowana komórka odpornościowa
- dłużej przywiera do komórek raka prostaty, przez co ma czas zainicjować proces ich zabijania,
- wydziela więcej substancji cytotoksycznych niszczących guz,
- lepiej się namnaża w trudnym środowisku nowotworu,
- wolniej ulega tzw. wyczerpaniu, czyli utracie zdolności do walki po długim kontakcie z rakiem.
Co ważne, w analizach publikowanych w „Science” nie odnotowano zwiększonego ataku na zdrowe tkanki. Precyzja rozpoznania komórki guza została utrzymana, a zmiana dotyczyła sposobu trzymania ofiary, nie samego wyboru celu.
Jedna modyfikacja aminokwasu zamieniła „zmęczonego strażnika” w znacznie skuteczniejszego zabójcę komórek nowotworowych – bez utraty selektywności.
Wyniki badań na myszach: guzy hamują wzrost, a czasem całkiem się zatrzymują
Najciekawsze dane pochodzą z testów na zwierzętach. U myszy z wszczepionym rakiem prostaty porównano dwa rodzaje terapii: podanie zwykłych limfocytów T oraz wstrzyknięcie komórek zmodyfikowanych metodą „catch bond engineering”.
Efekt był wyraźny. U zwierząt, które otrzymały „wzmocnione” limfocyty, wzrost guzów wyraźnie spowalniał, a w wielu przypadkach zdawał się całkowicie zatrzymywać. W grupie kontrolnej, z klasycznymi limfocytami T, guzy praktycznie nie reagowały na terapię.
Analiza tkanek wykazała też, że zmodyfikowane limfocyty T dłużej utrzymywały się w obrębie nowotworu i pozostawały w stanie aktywnym. Zwykle komórki odpornościowe w otoczeniu guza stopniowo „gasną”: przestają wydzielać substancje cytotoksyczne, gorzej się dzielą, nie reagują już na pobudzenie. W tej technologii udało się ten proces wyraźnie odsunąć w czasie.
Szansa nie tylko dla prostaty
Chociaż badania skupiają się na raku prostaty i receptorze rozpoznającym PAP, sama idea jest znacznie szersza. W wielu nowotworach litych – jak rak trzustki, jelita grubego czy niektóre guzy płuc – immunoterapia zawodzi między innymi dlatego, że limfocyty T nie potrafią utrzymać mocnego kontaktu z komórką raka.
Jeśli uda się wskazać inne „słabe” receptory na limfocytach i wzmocnić je w ten sam sposób, technika może stać się fundamentem całej nowej klasy terapii. Badacze mówią wprost o potencjale zastosowania w wielu typach nowotworów opornych na obecnie stosowane leki i przeciwciała.
Inżynieria haczyków nie celuje w konkretny nowotwór, ale w fundamentalną słabość połączenia między limfocytem T a komórką guza – dlatego tak kusi wizją szerszego zastosowania.
Co ta metoda może oznaczać dla pacjentów w przyszłości
Nie ma jeszcze mowy o rutynowym leczeniu ludzi tą technologią, potrzebne są lata dodatkowych badań. Naukowcy muszą sprawdzić bezpieczeństwo długotrwałego wzmacniania wiązania między limfocytem a komórką. Trzeba mieć pewność, że zmodyfikowane komórki nie zaczną mimo wszystko atakować zdrowych tkanek, na przykład pod wpływem stanów zapalnych czy innych chorób.
Jeśli kolejne etapy przyniosą podobnie obiecujące wyniki, taka terapia mogłaby uzupełnić obecne podejścia, takie jak klasyczna immunoterapia z użyciem przeciwciał, hormonoterapia czy chemioterapia. Część pacjentów z zaawansowanym rakiem prostaty nie reaguje na dostępne leczenie albo traci na nie odpowiedź po pewnym czasie. Dla nich każda metoda, która zatrzyma progresję choroby przy akceptowalnych skutkach ubocznych, ma ogromne znaczenie.
| Element terapii | Tradycyjne limfocyty T | Limfocyty T z „haczykiem” |
|---|---|---|
| Czas przylegania do komórki raka | krótki, łatwo dochodzi do odłączenia | wydłużony, połączenie wzmacnia się pod napięciem |
| Aktywność w obrębie guza | wygasa po dłuższej ekspozycji | utrzymuje się dłużej, komórki rzadziej się „męczą” |
| Skuteczność w modelach zwierzęcych | niewielki wpływ na wzrost guza | znaczne spowolnienie lub zatrzymanie wzrostu |
Immunoterapia, limfocyty T, aminokwasy – co warto wiedzieć, żeby zrozumieć tę koncepcję
Immunoterapia to ogólne określenie metod, które próbują wykorzystać własny układ odpornościowy pacjenta do walki z nowotworem. Zamiast atakować komórki raka „z zewnątrz” toksycznym lekiem, lekarze starają się odblokować lub wzmocnić naturalne mechanizmy obronne organizmu.
Limfocyty T pełnią w tym systemie rolę wyspecjalizowanych żołnierzy. Na ich powierzchni znajdują się receptory TCR, które rozpoznają fragmenty białek prezentowanych przez inne komórki. Jeśli limfocyt wychwyci coś niepokojącego – na przykład białko typowe dla raka – powinien uruchomić proces niszczenia podejrzanej komórki.
Aminokwas to jeden z „klocków”, z których zbudowane są białka. Zmiana zaledwie jednego elementu może zmodyfikować ruchomość, elastyczność czy wytrzymałość całego białka w określonym punkcie. Tu właśnie tak się stało: receptor zachował swoją „adresację” na raka prostaty, ale zyskał mechanicznie mocniejszy chwyt.
Dla pacjenta takie szczegóły biochemiczne brzmią często abstrakcyjnie. W praktyce mogą przełożyć się na prostą różnicę: albo immunoterapia daje minimalny efekt, albo zaczyna realnie kontrolować guz, wydłużając przeżycie czy poprawiając komfort życia.
Ryzyka, pytania i możliwe kolejne kroki
Każda ingerencja w układ odpornościowy, zwłaszcza tak głęboka, niesie potencjalne ryzyka. Najczęściej wymienia się trzy zagrożenia: reakcje autoimmunologiczne, nadmierne zapalenie oraz utrudnione wyłączenie terapii w razie powikłań. Modyfikacja, która sprawia, że limfocyt T lepiej trzyma się guza, nie może sprawić, że równie mocno „przyklei się” do zdrowej tkanki z lekko zmienionym białkiem.
Dlatego kolejne etapy rozwoju tej technologii zapewne obejmą:
- testy bezpieczeństwa na różnych modelach zwierzęcych,
- sprawdzanie, czy w innych chorobach białko docelowe nie pojawia się w pobliżu zdrowych tkanek,
- próby połączenia tej metody z innymi formami leczenia, np. z terapią hormonalną czy klasyczną chemioterapią,
- opracowanie sposobu „wyłączenia” zmodyfikowanych komórek w razie niepożądanej reakcji.
Dla osób żyjących z rakiem prostaty ta technologia to na razie laboratorna ciekawostka, ale wpisuje się w szerszy trend: przechodzenie z terapii ogólnoustrojowych, o dużej toksyczności, w kierunku bardzo precyzyjnych, komórkowych interwencji. Jeżeli takie podejście sprawdzi się w praktyce, w przyszłości leczenie może wyglądać zupełnie inaczej – mniej skojarzyć się z „bombardowaniem” raka, a bardziej z chirurgią na poziomie pojedynccych komórek.