Przełom w leczeniu raka gardła związanego z HPV: naukowcy „odsłaniają” oporne guzy
Uczeni z ośrodków w Stanach Zjednoczonych namierzyli jedną konkretną białkową „przełączkę”, dzięki której nowotwór staje się niewidzialny dla układu odpornościowego. Gdy udało się ją wyłączyć w modelach zwierzęcych, oporne wcześniej guzy nagle zaczęły znikać.
Raki głowy i szyi związane z HPV – cicha epidemia
W oddziałach onkologii laryngologicznej coraz częściej rozpoznaje się nowotwory gardła i jamy ustnej związane z zakażeniem wirusem brodawczaka ludzkiego (HPV). W Stanach Zjednoczonych lekarze mówią już o skalach zbliżonych do epidemii, a podobny trend widać w wielu krajach rozwiniętych.
Choć do arsenału leczenia dołączyła immunoterapia, część tych guzów praktycznie nie reaguje na nowoczesne leki. Chodzi zwłaszcza o terapie stosujące przeciwciała blokujące punkt kontrolny PD‑1, które mają „odhamować” limfocyty T i skierować je na komórki nowotworowe.
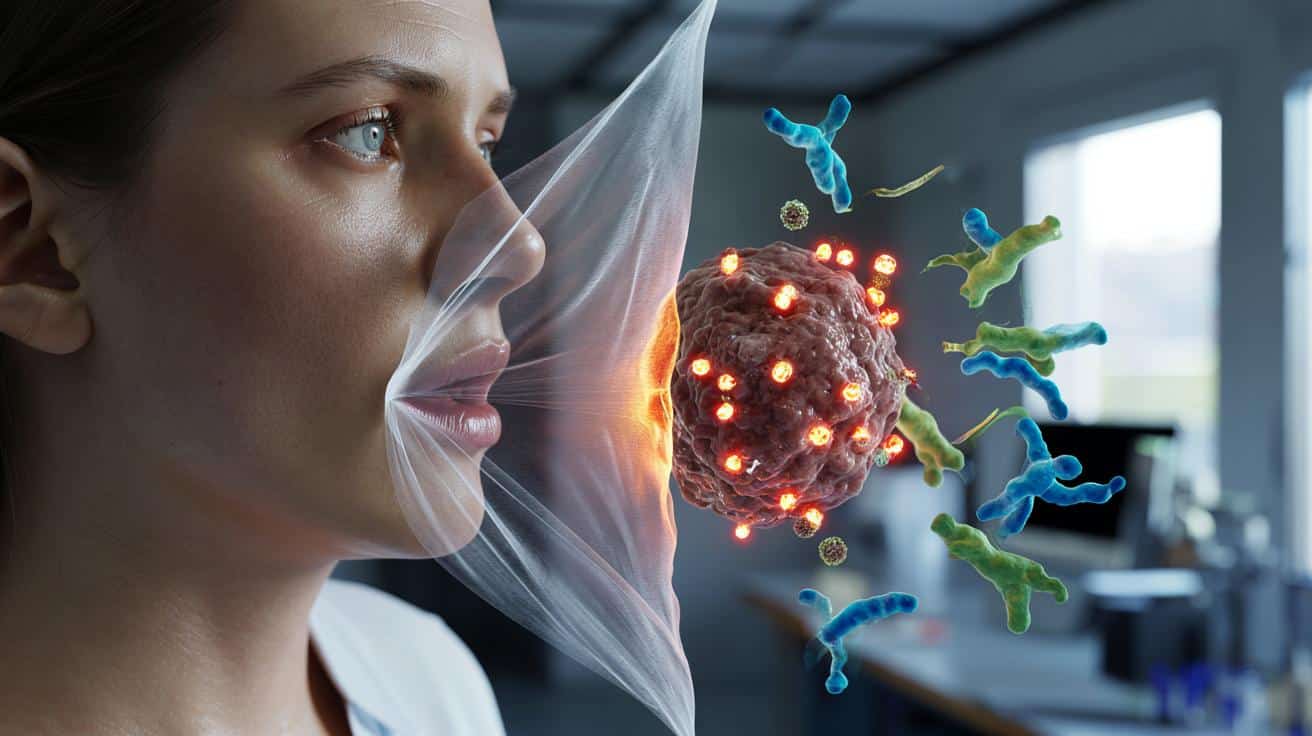
Nowotwory HPV-zależne głowy i szyi często zachowują się, jakby były otulone płaszczem niewidką – układ odpornościowy przechodzi obok nich obojętnie, a leki nie mają do czego „przycelować”.
Źródłem problemu jest brak odpowiednich sygnałów ostrzegawczych na powierzchni komórek rakowych. Bez nich limfocyty T czy komórki NK nie wiedzą, które komórki należy zniszczyć.
Jak HPV „wymazuje” nowotwór z radaru odporności
Zdrowe komórki prezentują na swojej powierzchni białka należące do układu zgodności tkankowej klasy I (MHC I). To coś w rodzaju identyfikatora: układ odpornościowy widzi, co się w komórce dzieje, i potrafi wychwycić nieprawidłowości. Komórki nowotworowe związane z HPV bardzo często pozbawione są tych cząsteczek albo mają ich śladową ilość.
W praktyce oznacza to, że:
- limfocyty T CD8+ nie rozpoznają komórek rakowych jako zagrożenia,
- komórki NK dostają mniej sygnałów, aby zaatakować,
- immunoterapia checkpoint inhibitorami działa słabiej, bo „odblokowane” limfocyty nadal nie widzą celu.
Do niedawna nie było jasne, jak dokładnie HPV doprowadza do tak dużego spadku ilości MHC I na komórkach nowotworowych. Zespół z Henry Ford Health i Michigan State University Health Sciences wskazał palcem konkretną cząsteczkę: białko MARCHF8.
Kluczowa rola białka MARCHF8 – nowotwór staje się niewidzialny
Naukowcy opisali mechanizm, w którym infekcja HPV „przekierowuje” MARCHF8 do usuwania z powierzchni komórek właśnie tych białek, które są niezbędne do rozpoznania przez układ odpornościowy. Komórka rakowa staje się przez to dużo trudniejsza do zidentyfikowania.
Gdy HPV uruchamia MARCHF8, komórka nowotworowa dosłownie zrzuca z siebie sygnały alarmowe MHC I. Dla układu odpornościowego zaczyna wyglądać jak element tła, a nie wroga struktura.
Badacze wyłączyli MARCHF8 w eksperymentalnych modelach raka HPV-dodatniego. W momencie, gdy ilość MHC I na powierzchni komórek wróciła do normy, limfocyty T i komórki NK natychmiast ruszyły do ataku. Co szczególnie ważne, działo się tak również w guzach, które wcześniej nie reagowały na klasyczne leczenie immunologiczne z użyciem przeciwciał anty‑PD‑1.
„Zimne” guzy zamieniają się w „gorące”
Onkolodzy często używają określeń „zimne” i „gorące” guzy. Te pierwsze są słabo nacieczone przez komórki odpornościowe, przez co reagują marnie na immunoterapię. Te drugie są pełne limfocytów i komórek NK – leki tylko wzmacniają już istniejącą odpowiedź.
Według badaczy wyłączenie MARCHF8 sprawiło, że guzy dotąd „zimne” zaczęły zachowywać się jak „gorące”. W modelach zwierzęcych zaobserwowano:
| Co zmierzono | Co się wydarzyło po wyłączeniu MARCHF8 |
|---|---|
| Obecność MHC I na komórkach raka | Wyraźny wzrost, powrót sygnałów alarmowych |
| Liczba limfocytów T w guzie | Silny napływ aktywnych limfocytów CD8+ |
| Obecność komórek NK i makrofagów | Zdecydowany przyrost w mikrośrodowisku guza |
| Komórki o działaniu immunosupresyjnym | Spadek ich udziału w obrębie guza |
| Wielkość i tempo wzrostu guza | Silne hamowanie rozwoju, w części przypadków brak guza |
Połączenie blokady MARCHF8 z klasycznym lekiem anty‑PD‑1 dało u części zwierząt całkowitą remisję bez nawrotu w obserwowanym okresie. To sygnał, że nowy cel terapeutyczny może znacząco poprawić skuteczność już dostępnych metod.
Nowy cel dla leków – co może z tego wyniknąć dla pacjentów
Autorzy badań podkreślają, że ich praca koncentrowała się na modelach raka związanych z HPV. Ta grupa chorych często ma ograniczone opcje, gdy guzy przestają reagować na radioterapię, chemioterapię czy standardową immunoterapię.
Zahamowanie MARCHF8 może otworzyć drzwi do zupełnie nowej kombinacji terapii – leku celującego w „ukrywanie się” nowotworu i immunoterapii wzmacniającej atak limfocytów T oraz komórek NK.
Teraz badacze chcą przejść od manipulacji genetycznych w laboratorium do stworzenia realnego leku dla ludzi. Chodzi o cząsteczkę, która zablokuje MARCHF8 w komórkach nowotworowych, przywróci im ekspresję MHC I i wzmocni reakcję na istniejące terapie.
Droga od laboratorium do szpitala
Przeskok z badań na myszach do terapii u ludzi jest zawsze długi i pełen znaków zapytania. Zanim potencjalny lek trafi do pacjentów, trzeba sprawdzić kilka kluczowych kwestii:
- czy blokowanie MARCHF8 jest bezpieczne dla zdrowych tkanek,
- jaką dawkę toleruje organizm,
- czy efekt będzie podobny u ludzi jak w modelach zwierzęcych,
- z jakimi immunoterapiami blokada MARCHF8 działa najlepiej,
- czy mechanizm sprawdzi się też w innych nowotworach z niską ilością MHC I.
Dopiero po serii badań przedklinicznych i wczesnych badań klinicznych można będzie mówić o rutynowym zastosowaniu u chorych. Mimo to samo zidentyfikowanie białka, które wprost odpowiada za „wyciszanie” sygnałów alarmowych, daje nadzieję na bardziej celowane strategie leczenia.
Dlaczego rak związany z HPV jest coraz częstszy
Rak gardła i części ustnej powiązany z HPV zwykle nie ma nic wspólnego z paleniem papierosów czy nadużywaniem alkoholu, które przez lata kojarzyły się z nowotworami głowy i szyi. Kluczową rolę odgrywa tu zakażenie onkogennymi typami HPV, przenoszone głównie drogą kontaktów seksualnych.
Szczepionki przeciw HPV, stosowane od lat w profilaktyce raka szyjki macicy, zmniejszają także ryzyko późniejszych nowotworów jamy ustnej i gardła. Wciąż jednak wiele osób nie jest zaszczepionych, a świadomość związku między HPV a rakiem poza narządami płciowymi pozostaje niska.
Dla pacjentów, u których rak już się rozwinął i okazał się odporny na leczenie, prace nad MARCHF8 dają nową perspektywę. Możliwe, że za kilka lat chorzy, którzy dziś słyszą, że wykorzystano wszystkie dostępne opcje, dostaną jeszcze jedną szansę.
Co to znaczy dla zwykłego pacjenta
Nie każdy musi znać szczegóły działania MHC I czy limfocytów CD8+. Dla osoby, która w rodzinie ma przypadki raka głowy i szyi, liczy się przede wszystkim kilka faktów:
- coraz lepiej rozumiemy, jak nowotwory „oszukują” odporność,
- pojawiają się nowe cele dla leków, obok klasycznej chemioterapii i radioterapii,
- szczepienie przeciw HPV to realne zmniejszenie ryzyka choroby w przyszłości,
- chorzy z opornymi guzami mogą w przyszłości kwalifikować się do terapii łączonych, które dziś dopiero są projektowane.
Warto też mieć na uwadze, że rak głowy i szyi na wczesnym etapie często daje niespecyficzne objawy: przewlekłe bóle gardła, chrypkę, uczucie przeszkody przy połykaniu, niegojące się owrzodzenia w jamie ustnej, powiększone węzły chłonne szyi. Dłużej utrzymujące się dolegliwości powinny skłonić do wizyty u lekarza laryngologa lub onkologa.
Z punktu widzenia medycyny personalizowanej badania nad MARCHF8 to kolejny krok w kierunku terapii szytych na miarę biologii konkretnego guza. Zamiast podawać wszystkim pacjentom te same schematy, lekarze coraz częściej starają się zrozumieć, dlaczego dany nowotwór nie reaguje na leczenie – i uderzyć właśnie w ten mechanizm. Jeśli w HPV-zależnych rakach głowy i szyi chodzi głównie o „ukrywanie się” przed odpornością, blokada MARCHF8 może stać się jednym z najciekawszych kierunków rozwoju onkologii w najbliższych latach.