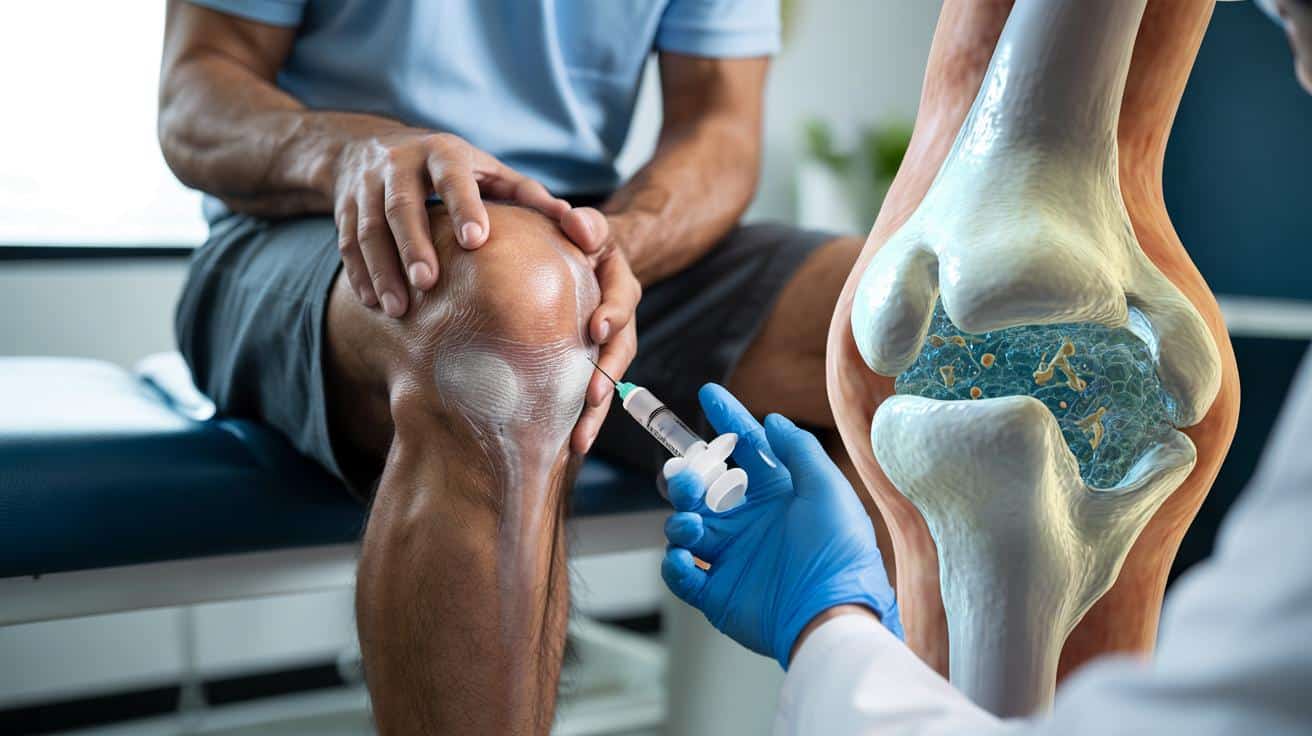
Przełom w leczeniu kolan: naprawa chrząstki bez sztucznej protezy
Medycyna szykuje im jednak zupełnie inną przyszłość.
Nowe metody leczenia nie skupiają się już tylko na łagodzeniu bólu. Naukowcy próbują przywrócić chrząstce zdolność do samonaprawy, czyli zrobić coś, co jeszcze niedawno wydawało się całkowicie nierealne. Dwie niezależne prace badawcze pokazują, że taki scenariusz przestaje być czystą teorią.
Dlaczego chrząstka w kolanie prawie się nie goi
Chrząstka stawowa pokrywa końce kości, działa jak zderzak i smar jednocześnie. Jest gładka, sprężysta i niemal bez tarcia. Gdy ulega zniszczeniu, zaczyna się klasyczna historia pacjenta z chorobą zwyrodnieniową stawów: ból przy chodzeniu, sztywność, ograniczenie ruchu, potem zastrzyki, silne leki, wreszcie operacja i ciężka proteza.
Ten scenariusz wynika z jednej cechy biologii: chrząstka prawie wcale się nie odnawia. Ma skąpe ukrwienie i niewiele komórek zdolnych do naprawy uszkodzeń. Dzisiejsza ortopedia potrafi wymienić zużyty staw, ale nie przywrócić go do naturalnego stanu. Nowe podejścia uderzają w ten problem z dwóch zupełnie różnych stron.
Naukowcy chcą, by zamiast wymieniać kolano na metal i plastik, lekarz mógł wstrzyknąć preparat, który pobudzi organizm do odtworzenia własnej, trwałej chrząstki.
Odmładzanie chrząstki blokadą enzymu starzenia
Zespół badawczy z prestiżowego ośrodka w Stanach Zjednoczonych skupił się na jednym białku, którego poziom w stawach rośnie wraz z wiekiem. To enzym o nazwie 15-PGDH, odpowiedzialny za rozkładanie prostaglandyny E2 – cząsteczki ważnej dla procesów regeneracji tkanek.
Badacze postawili prostą tezę: jeśli da się zahamować ten enzym, prostaglandyna dłużej utrzyma się w stawie, a chrząstka odzyska część młodzieńczych zdolności naprawczych. Sprawdzili to na myszach w podeszłym wieku, wstrzykując do ich kolan inhibitor 15-PGDH.
Efekt okazał się zaskakująco mocny. Komórki chrząstki – chondrocyty – zaczęły zachowywać się jak u młodszych osobników. Zmienił się ich profil genetyczny i rodzaj wytwarzanej tkanki.
- odsetek komórek produkujących tzw. chrząstkę szklistą wzrósł z 22% do 42%
- liczba komórek tworzących słabszą chrząstkę włóknistą spadła mniej więcej o połowę
- tkanka miała strukturę bliższą zdrowej, naturalnej powierzchni stawowej
Chrząstka szklista jest kluczowa, bo właśnie ten typ buduje gładką, odporną na ścieranie powierzchnię stawową. Chrząstka włóknista, która zwykle powstaje po urazach czy zabiegach, jest twardsza, ale mniej elastyczna i szybciej się niszczy.
Pierwsze wyniki także na ludzkiej tkance
Badacze nie zatrzymali się na modelu zwierzęcym. Zastosowali tę samą strategię na fragmentach ludzkiej chrząstki pobranej podczas zabiegów wymiany kolana. Po tygodniu ekspozycji na inhibitor enzymu pojawiły się wyraźne oznaki odnowy tkanek.
Blokada jednego enzymu zaczęła przeprogramowywać „stare” chondrocyty na bardziej młodzieńczy tryb pracy, bez przeszczepów i bez komórek macierzystych.
Co ważne dla przyszłych pacjentów, wczesna faza badań klinicznych z użyciem tego typu inhibitorów u zdrowych ochotników wykazała, że preparat jest dobrze tolerowany. To jeszcze nie terapia na receptę, ale ważny krok na drodze do wstrzykiwanej „kuracji odmładzającej” kolana.
Specjalny żel, który w stawie zamienia się w rusztowanie dla nowej chrząstki
Druga praca badawcza idzie w przeciwną stronę. Zamiast pobudzać komórki przez blokadę enzymu, naukowcy zaprojektowali nowy materiał, który ma zastąpić brakującą chrząstkę i jednocześnie zachęcić komórki do odtwarzania prawidłowej struktury.
To biomateriał opracowany na uniwersytecie w Stanach Zjednoczonych, złożony z dwóch elementów: krótkiego fragmentu białka o działaniu biologicznym i zmodyfikowanego kwasu hialuronowego, dobrze znanego z maści i zastrzyków na stawy. Po połączeniu tworzą one samoukładające się nanowłókna, które przypominają sieć występującą w naturalnej chrząstce.
Preparat ma konsystencję gęstego żelu. Po wstrzyknięciu do stawu spotyka się z jonami wapnia i tam, na miejscu, zmienia się w miękką, ale wytrzymałą strukturę. Powstaje coś w rodzaju trójwymiarowego rusztowania z porami, w które mogą wnikać komórki pacjenta.
Testy na zwierzętach: nowa chrząstka w pół roku
Tak przygotowany materiał przetestowano na owcach z rozległymi ubytkami chrząstki w stawie podobnym do ludzkiego kolana. Po sześciu miesiącach w miejscach uszkodzeń zaczęła się tworzyć nowa tkanka o parametrach zbliżonych do zdrowej chrząstki stawowej: z obecnością kolagenu typu II i proteoglikanów, które odpowiadają za sprężystość i odporność na ściskanie.
W odróżnieniu od popularnej techniki mikrofraktury, nowy żel sprzyja tworzeniu pełnowartościowej chrząstki szklistej, a nie tylko gorszej jakości „łaty” z chrząstki włóknistej.
Mikrofraktura, czyli nawiercanie kości pod chrząstką, to dziś jedna z częstszych metod stosowanych u młodszych, aktywnych pacjentów z ograniczonym ubytkiem chrząstki. Daje ulgę, ale nie ma gwarancji, że efekt utrzyma się długo – naprawczy materiał jest po prostu słabszy. Biomateriał z uniwersytetu został zaprojektowany tak, by ten problem wyeliminować.
Następny krok: testy u ludzi
Zespół odpowiedzialny za ten żel szykuje dokumentację, by uzyskać zgodę amerykańskiego regulatora na pierwsze badania kliniczne u pacjentów. Jeśli wszystko pójdzie zgodnie z planem, w perspektywie kilku lat pierwsi chorzy z zaawansowaną chorobą zwyrodnieniową mogliby otrzymać zamiast zabiegu chirurgicznego serię iniekcji biomateriału.
| Strategia | Co robi | Potencjalny efekt dla pacjenta |
|---|---|---|
| Blokada 15-PGDH | Odblokowuje naturalne procesy naprawcze chrząstki związane z wiekiem | Odmłodzenie tkanki, spowolnienie lub odwrócenie zmian zwyrodnieniowych |
| Biomateriał w formie żelu | Daje komórkom rusztowanie, na którym mogą odbudować prawidłową chrząstkę | Wypełnienie ubytku mocną, funkcjonalną chrząstką szklistą |
Szansa na odłożenie endoprotezy o wiele lat
Choroba zwyrodnieniowa stawów to jedna z najczęstszych przyczyn bólu i niepełnosprawności. W samych Stanach Zjednoczonych dotyczy około jednej piątej dorosłych i generuje dziesiątki miliardów dolarów wydatków medycznych rocznie. W Europie jest podobnie – w krajach takich jak Francja problemy z chrząstką ma ponad 10 milionów osób.
Aktualne leczenie jest mocno ograniczone. Lekarze mogą łagodzić ból środkami przeciwzapalnymi, zalecać rehabilitację i odciążenie stawu. W pewnym momencie wachlarz możliwości się kończy i pojawia się propozycja wymiany stawu na endoprotezę. To operacja kosztowna, obciążająca dla organizmu, wymagająca długiej rehabilitacji i niepozbawiona ryzyka powikłań.
Jeżeli opisane terapie przejdą pełną ścieżkę badań klinicznych z pozytywnym wynikiem, schemat leczenia może wyglądać zupełnie inaczej. Zamiast czekać, aż chrząstka zniszczy się do końca, lekarz mógłby znacznie wcześniej zaproponować serię iniekcji, które mają zatrzymać proces niszczenia, a nawet odbudować utraconą tkankę.
Co mogą oznaczać te badania dla przeciętnej osoby z bolącym kolanem
Dla dzisiejszego pacjenta z kolanem „do wymiany” te projekty to jeszcze pieśń przyszłości. Obie metody są na etapie przed wdrożeniem do rutynowej praktyki, a prawdziwy sprawdzian dopiero nadejdzie, gdy zderzą się z różnorodnością prawdziwych przypadków: innym stanem zdrowia, masą ciała, poziomem aktywności.
Mimo to warto rozumieć, jakiego typu korzyści mogą się pojawić:
- szansa na odsunięcie protezy w czasie, zwłaszcza u osób w średnim wieku
- mniejsze uzależnienie od leków przeciwbólowych i przeciwzapalnych
- krótszy powrót do sprawności po leczeniu w porównaniu z operacją
- więcej możliwości indywidualnego dopasowania terapii do stopnia zniszczenia stawu
Warto też pamiętać o ciemniejszych stronach. Każda nowa metoda wiąże się z ryzykiem działań niepożądanych, kosztami i brakiem gwarancji skuteczności u wszystkich pacjentów. Blokowanie enzymów ingeruje w delikatne sieci sygnałów biologicznych, a wszczepiane materiały muszą przez lata zachowywać stabilność i nie wywoływać reakcji zapalnych.
Dla osób zmagających się dziś z bólem stawów praktyczne wnioski pozostają niezmienne: dbałość o masę ciała, wzmacnianie mięśni wokół stawu, unikanie przeciążeń i szybkie reagowanie na pierwsze objawy wciąż stanowią najbardziej dostępne „terapie regeneracyjne”. Nowe metody mogą kiedyś dołączyć do tego zestawu jako kolejne narzędzie lekarza – tym razem zdolne nie tylko uśmierzyć ból, ale rzeczywiście przywrócić kolanu sprawność na dłużej.