Alzheimer może brać się z „walki” białek w mózgu, nie z blaszek
Nowa hipoteza naukowców z Kalifornii stawia na głowie dotychczasowe myślenie o tym, skąd tak naprawdę bierze się Alzheimer.
Przez lata lekarze obwiniali głównie złogi białek odkładające się w mózgu osób starszych. Najnowsze badania sugerują jednak, że kluczowe wydarzenia rozgrywają się znacznie głębiej – wewnątrz pojedynczej komórki nerwowej, gdzie dwa białka ścierają się o kontrolę nad jej systemem transportowym.
Nie tylko „blaszki w mózgu”. Naukowcy proponują inną przyczynę
Badacze z Uniwersytetu Kalifornijskiego w Riverside przeanalizowali zachowanie dwóch dobrze znanych białek związanych z chorobą Alzheimera: beta-amyloidu oraz tau. Oba od dawna pojawiają się w opisach patologii tej choroby, lecz zwykle rozpatrywano je osobno – jedne zespoły badawcze skupiały się na beta-amyloidzie, inne na tau.
Nowe prace pokazują, że taka separacja może zniekształcać obraz. Kluczowe może być to, jak te dwie cząsteczki oddziałują ze sobą w tej samej neuronie. Zamiast spokojnej koegzystencji mamy coś w rodzaju molekularnej rywalizacji o to, kto będzie „rządził” mikrotubulami, czyli strukturami odpowiedzialnymi za transport wewnątrz komórek nerwowych.
Badanie sugeruje, że choroba rozwija się, gdy beta-amyloid zaczyna wypierać białko tau z mikrotubul i paraliżuje transport w neuronie.
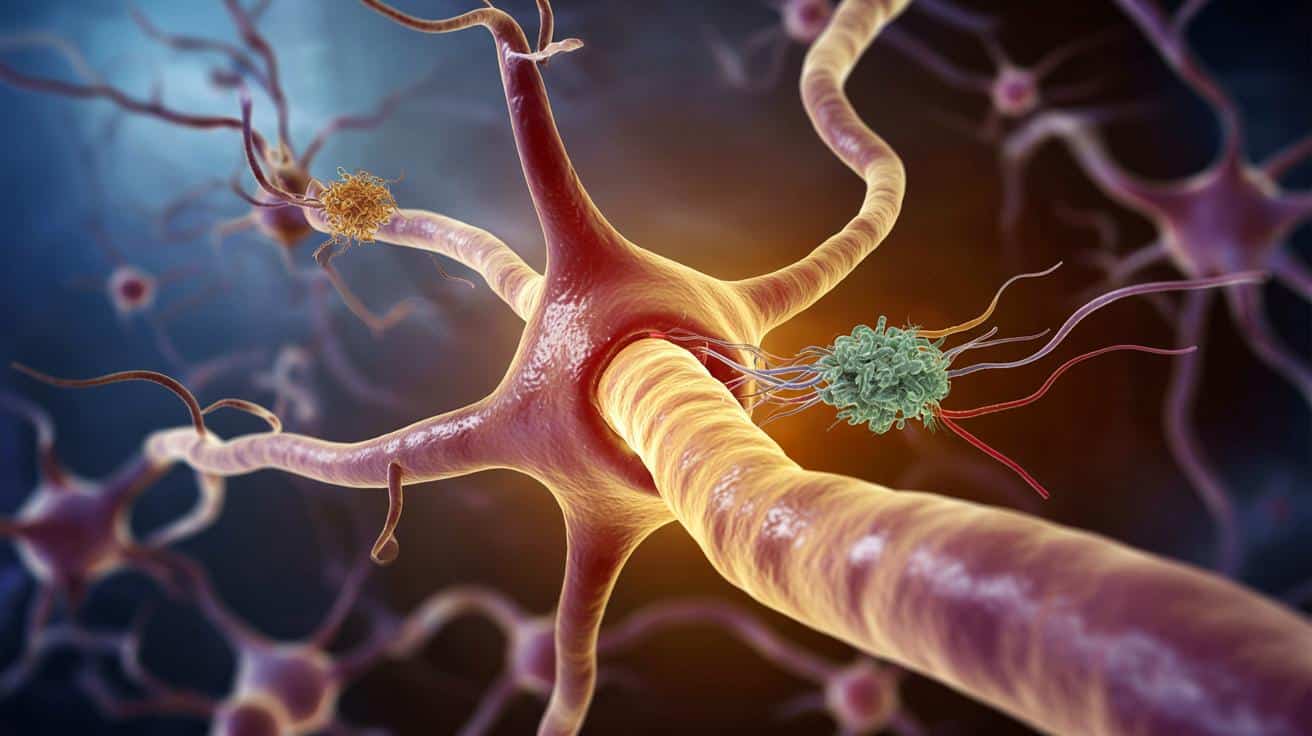
Co to są mikrotubule i dlaczego są tak ważne dla pamięci
Mikrotubule można sobie wyobrazić jak system wewnętrznych autostrad w każdej komórce nerwowej. Po tych „drogach” poruszają się pęcherzyki z substancjami odżywczymi, białkami, neurotransmiterami. Bez sprawnego transportu aksony i dendryty nerwów stopniowo obumierają, a komunikacja między komórkami się załamuje.
Rolę drogówki na tych autostradach pełni białko tau. Stabilizuje mikrotubule, wzmacnia je i dba o to, by struktury nie rozpadały się zbyt szybko. Dzięki temu neurony mogą funkcjonować przez dziesiątki lat, mimo ogromnego obciążenia.
Naukowcy z Kalifornii zauważyli, że fragmenty tau, które wiążą się z mikrotubulami, są zaskakująco podobne do fragmentów innego słynnego białka – beta-amyloidu. Podobieństwo dotyczy zarówno wielkości, jak i budowy przestrzennej. To zapaliło badaczom czerwone światło: jeśli fragmenty są tak podobne, to może rywalizują o te same miejsca w mikrotubulach.
Beta-amyloid wchodzi na cudzy teren
Aby to sprawdzić, zespół wykorzystał znakowane fluorescencyjnie wersje białek, obserwując pod mikroskopem, co dokładnie przykleja się do mikrotubul. Wynik był jasny: beta-amyloid faktycznie przyłącza się do mikrotubul, i to z siłą bardzo zbliżoną do tau.
Gdy w neuronie gromadzi się zbyt dużo beta-amyloidu, zaczyna on zajmować miejsca przewidziane dla tau, osłabiając „szkielet” komórki nerwowej.
W praktyce oznacza to, że system transportowy neuronu traci stabilność. Pęcherzyki z ważnymi cząsteczkami nie docierają tam, gdzie powinny. Z czasem takie komórki zaczynają gorzej przewodzić impulsy, a następnie obumierają. Krótko mówiąc – pamięć i zdolności poznawcze stopniowo się sypią.
Dlaczego dotychczasowe terapie często nie działają
Od dekad trwają próby leczenia Alzheimera przez usuwanie złogów beta-amyloidu z mózgu. Tysiące pacjentów wzięło udział w badaniach klinicznych, wiele leków spektakularnie zawiodło. W części przypadków udawało się zmniejszyć ilość blaszek w mózgu, ale stan chorych nie poprawiał się tak, jak oczekiwano.
Nowa koncepcja może tłumaczyć ten paradoks. Zewnętrzne złogi beta-amyloidu, widoczne na obrazach mózgu, mogą być tylko skutkiem ubocznym procesu, który naprawdę szkodzi neuronom. Kluczowe szkody powstają wcześniej, gdy beta-amyloid wewnątrz komórki zaczyna przejmować kontrolę nad mikrotubulami.
Jeśli tak jest, to samo usuwanie blaszek na zewnątrz neuronów nie wystarczy. Część komórek nerwowych może być już „martwa od środka”, bo ich system transportowy rozpadł się dużo wcześniej.
Jak wiek i „sprzątanie” komórek mieszają w tej układance
Zespół z Riverside zwraca uwagę na jeszcze jeden ważny element: wiek i sprawność autofagii. Autofagia to wewnętrzny mechanizm „sprzątania” w komórkach. Każdy neuron na bieżąco usuwa uszkodzone białka i inne śmieci, zanim zrobią bałagan.
Z wiekiem ten system coraz częściej się zacina. Niewy czyszczone białka gromadzą się – w tym beta-amyloid. Im więcej takiego materiału, tym większa szansa, że zacznie on zajmować miejsca tau na mikrotubulach.
- sprawna autofagia – beta-amyloid szybko usuwany, tau stabilizuje mikrotubule;
- osłabiona autofagia – beta-amyloid zalega, wypiera tau;
- długotrwałe zaburzenie – uszkodzony transport, neurony zaczynają obumierać.
Taki łańcuch zdarzeń dobrze pasuje do tego, co lekarze obserwują u pacjentów: powolny, rozciągnięty w czasie proces, który na początku prawie nie daje objawów, by po latach uderzyć pełnoobjawowym otępieniem.
Lit, mikrotubule i nowe cele dla leków
Ciekawy trop daje lit – pierwiastek znany głównie z leczenia choroby afektywnej dwubiegunowej. Nowsze analizy pokazały, że osoby przyjmujące lit w małych dawkach mogą mieć niższe ryzyko rozwoju Alzheimera. Nikt nie był jednak pewien, dlaczego tak się dzieje.
Starsze badania wskazywały, że lit stabilizuje mikrotubule. Jeśli więc najnowsza hipoteza z Kalifornii jest trafna, to lit może chronić neurony, wzmacniając ich wewnętrzne „rusztowanie” i utrudniając beta-amyloidowi przejęcie kontroli nad transportem.
Coraz więcej danych sugeruje, że ochrona mikrotubul i wsparcie mechanizmów sprzątania w komórkach mogą być skuteczniejszym celem niż samo polowanie na blaszki białkowe.
To przesuwa punkt ciężkości w projektowaniu terapii. Zamiast skupiać się wyłącznie na rozbijaniu agregatów beta-amyloidu, badacze mogą zacząć szukać:
- leków, które utrudnią beta-amyloidowi wiązanie się z mikrotubulami,
- substancji wzmacniających funkcję tau,
- strategii poprawiających autofagię, czyli sprzątanie wewnątrz neuronów.
Co z tego wynika dla zwykłego człowieka
Choć opis badań brzmi bardzo technicznie, w tle chodzi o coś bardzo przyziemnego – o to, czy uda się kiedyś skutecznie spowolnić lub zatrzymać chorobę, która niszczy pamięć milionów ludzi. Nowy model daje spójną „mapę”, która lepiej łączy wiele wcześniejszych, czasem sprzecznych wyników.
Dla osób dbających o zdrowie mózgu oznacza to także większe zainteresowanie czynnikami, które wpływają na autofagię i ogólne „sprzątanie” w komórkach. Coraz więcej badań mówi, że znaczenie mogą mieć m.in. aktywność fizyczna, sen, właściwa kontrola cukru we krwi czy unikanie przewlekłych stanów zapalnych. Każdy z tych elementów może pośrednio wspierać sprawność mechanizmów komórkowych.
Dlaczego ta hipoteza tak mocno przyciąga uwagę
Naukowcy od lat szukają spójnego wyjaśnienia, które połączy obecność blaszek beta-amyloidu, splątków tau i fakt, że wiele terapii nastawionych na jedno z tych zjawisk zawodzi. Koncepcja „rywalizacji” o mikrotubule porządkuje ten chaos. Pokazuje, że nie chodzi o dwa niezależne problemy, ale o ten sam front walki wewnątrz neuronu.
Dla medycyny to szansa na bardziej logiczne projektowanie badań klinicznych i testowanie leków, które celują w cały łańcuch zdarzeń, a nie tylko w najbardziej widoczny objaw w postaci blaszek na obrazach mózgu.
Z perspektywy pacjentów i ich rodzin ważne staje się jeszcze coś: im wcześniej uda się zahamować zaburzenia transportu w neuronie, tym większa szansa, że objawy choroby pojawią się później lub będą łagodniejsze. To z kolei zwraca uwagę na potrzebę wcześniejszej diagnostyki, śledzenia subtelnych zmian w funkcjach poznawczych i inwestowania w profilaktykę zanim uszkodzenia w mózgu staną się nieodwracalne.