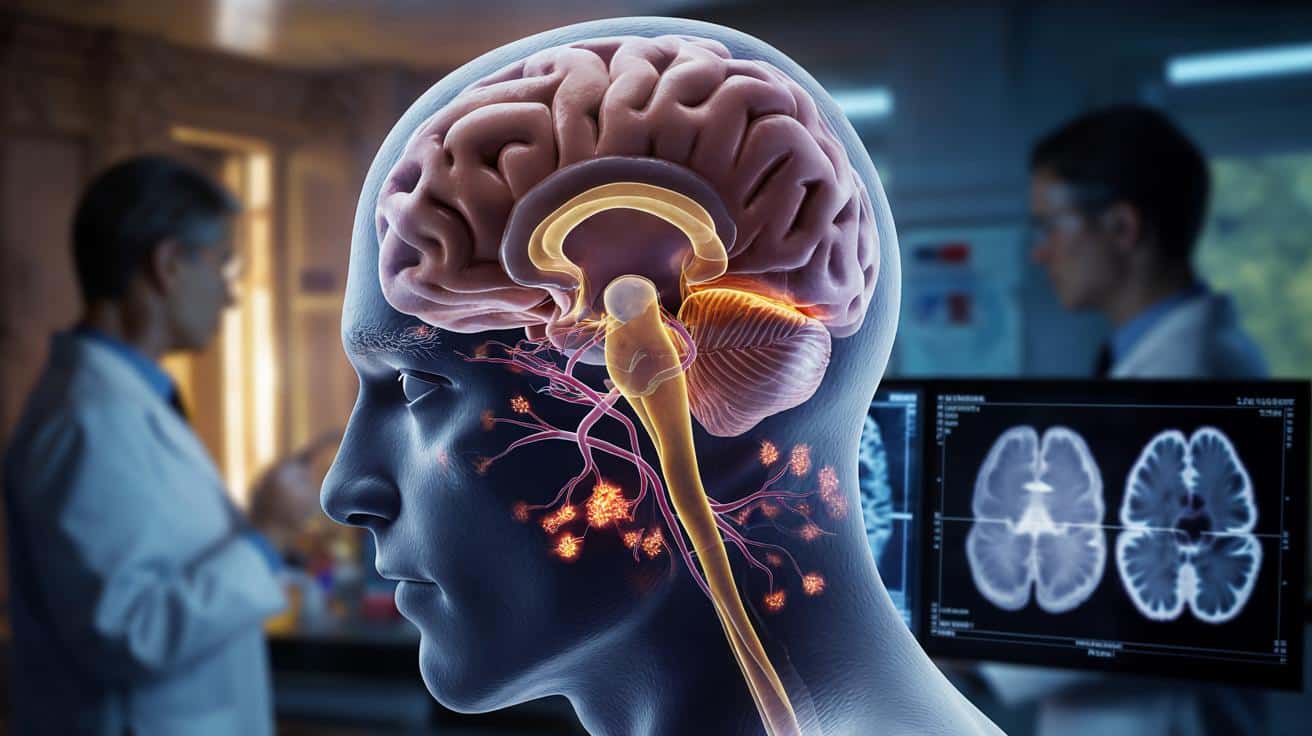
Alzheimer: francuscy naukowcy namierzają brakujące ogniwo w rozwoju choroby
Francuski zespół badawczy wskazał nowy mechanizm w mózgu, który może napędzać rozwój choroby Alzheimera i gromadzenie się białka Tau.
To nie jest kolejna ogólna hipoteza, ale wynik wieloletnich badań nad rzadko opisywaną grupą komórek mózgowych. Naukowcy z Lille pokazali, że te małe, pomijane dotąd struktury mogą sterować procesem, który u części osób kończy się otępieniem, utratą pamięci i samodzielności.
Choroba Alzheimera: ogromny problem, wciąż bez skutecznego leku
Choroba Alzheimera to najczęstsza przyczyna otępienia. Najczęściej dotyka osoby po 65. roku życia, częściej kobiety niż mężczyzn. We Francji żyje z nią około 900 tysięcy osób, w Polsce szacuje się co najmniej kilkaset tysięcy chorych, a realna liczba może być znacznie wyższa, bo wiele przypadków pozostaje nierozpoznanych.
Obraz kliniczny bywa podobny: stopniowe pogarszanie pamięci, kłopoty z orientacją, trudności w wykonywaniu prostych czynności, zmiany zachowania. W tle zachodzą procesy neurodegeneracyjne – mózg dosłownie kurczy się, a neurony tracą zdolność prawidłowego działania i obumierają.
Mimo głośnych doniesień o nowych lekach, wciąż nie dysponujemy terapią, która w sposób pewny i trwały zatrzymałaby chorobę u większości pacjentów. Stąd tak ogromne zainteresowanie nauki mechanizmami, które uruchamiają i podtrzymują uszkodzenia w mózgu.
Białko Tau – toksyczny znak rozpoznawczy choroby
W chorobie Alzheimera lekarze i naukowcy najczęściej mówią o dwóch charakterystycznych zjawiskach: złogach beta-amyloidu oraz patologicznej formie białka Tau. To drugie, Tau, odgrywa szczególnie niszczącą rolę we wnętrzu neuronów.
Patologiczne białko Tau gromadzi się w komórkach nerwowych, zaburza ich „szkielet” wewnętrzny, rozrywa połączenia i prowadzi do ich śmierci.
W zdrowym mózgu Tau stabilizuje mikrotubule, czyli swoiste rusztowanie, po którym transportowane są substancje niezbędne komórce. Gdy białko przyjmuje nieprawidłowy kształt i ulega nadmiernej modyfikacji chemicznej (np. fosforylacji), zaczyna się zlepiać w splątki. Te splątki to klasyczny obraz w badaniach neuropatologicznych mózgu chorej osoby.
Dotąd wiele zespołów badawczych skupiało się właśnie na samym białku Tau lub na beta-amyloidzie, próbując je bezpośrednio usuwać lub blokować ich tworzenie. Skuteczność takich strategii pozostaje ograniczona, więc pojawiło się pytanie: czy w mózgu istnieją inne „regulatory”, które sprzyjają powstawaniu patologicznego Tau?
Kim są tajemnicze tanycyty i gdzie je znaleźć
Zespół dr. Vincenta Prévota z ośrodka Lille Neurosciences et Cognition od ponad dwóch dekad interesuje się bardzo specyficzną grupą komórek – tanycytami. To wyspecjalizowane komórki glejowe, które znajdują się głównie w rejonie trzeciej komory mózgu, w pobliżu podwzgórza.
Tanycyty pełnią rolę pośrednika między krwią, płynem mózgowo-rdzeniowym a strukturami głębiej położonymi. Można je porównać do czujników i kurierów jednocześnie: monitorują skład chemiczny otoczenia i przekazują sygnały dalej, regulując m.in. gospodarkę energetyczną, apetyt czy funkcjonowanie hormonów.
Przez lata traktowano je głównie jako element układu neuroendokrynnego, czyli łączącego układ nerwowy z hormonalnym. Mało kto łączył je z procesami typowymi dla otępienia.
Nowy mechanizm: jak tanycyty wpływają na gromadzenie białka Tau
Badacze z Lille wykazali, że tanycyty nie są biernymi obserwatorami zmian w mózgu, ale aktywnie uczestniczą w procesie gromadzenia patologicznego białka Tau. Ich praca, opisana w renomowanym czasopiśmie naukowym, krok po kroku pokazuje, jak może wyglądać ten łańcuch zdarzeń.
Wyniki sugerują, że zaburzenia pracy tanycytów mogą sprzyjać temu, aby patologiczne Tau łatwiej przemieszczało się w mózgu i kumulowało tam, gdzie zadaje największe szkody.
Z przedstawionych danych wynika, że:
- tanycyty mogą wychwytywać białko Tau z płynu mózgowo-rdzeniowego,
- w określonych warunkach zmienia się ich zdolność do „sprzątania” lub neutralizowania tej cząsteczki,
- gdy mechanizm oczyszczania zawodzi, Tau może szybciej odkładać się w pobliskich strukturach, w tym w rejonach odpowiadających za pamięć i funkcje poznawcze.
Naukowcy zaobserwowali, że z wiekiem oraz przy toczących się procesach neurodegeneracyjnych tanycyty zmieniają swój kształt, aktywność i ekspresję określonych genów. Taka zmiana sprawia, że ich „strażnicza” rola słabnie, a mózg traci jedno z narzędzi obrony przed toksyczną formą Tau.
Dlaczego to może być przełom dla przyszłych terapii
W centrum uwagi znalazła się więc nowa kategoria celu terapeutycznego: nie samo białko Tau, lecz komórki, które kontrolują jego obecność i rozprzestrzenianie. Dla firm farmaceutycznych i zespołów badawczych to atrakcyjny kierunek, bo otwiera kilka możliwych strategii działania.
| Możliwy kierunek terapii | Co miałby robić |
|---|---|
| Wzmocnienie pracy tanycytów | Poprawa ich zdolności do usuwania patologicznego Tau z płynu mózgowo-rdzeniowego |
| Ochrona przed starzeniem | Spowolnienie zmian degeneracyjnych w tanycytach u osób w wieku podeszłym |
| Precyzyjne blokowanie szlaków sygnałowych | Zahamowanie procesów, które zwiększają przepuszczalność dla toksycznego Tau |
Taki sposób myślenia zmienia optykę: celem staje się środowisko, w którym neurony funkcjonują, a nie tylko same komórki nerwowe. Jeżeli uda się przywrócić równowagę w pracy tanycytów, istnieje szansa, że mózg lepiej poradzi sobie z „nadmiarem” patologicznego Tau, zanim to zniszczy sieć połączeń neuronów.
Jak ta wiedza może kiedyś trafić do gabinetu lekarskiego
Od opisania mechanizmu w badaniach laboratoryjnych do gotowego leku droga jest daleka. Konieczne będą eksperymenty na modelach zwierzęcych, a później dobrze zaprojektowane badania kliniczne u ludzi. Mimo to już teraz można wskazać kilka potencjalnych praktycznych konsekwencji tej pracy.
- Rozwój nowych biomarkerów – jeśli tanycyty zmieniają aktywność na wczesnym etapie choroby, być może da się to wykryć w płynie mózgowo-rdzeniowym lub we krwi, zanim dojdzie do dużych uszkodzeń mózgu.
- Lepsze planowanie terapii – przyszłe leki mogą łączyć działanie na beta-amyloid, Tau i środowisko komórkowe, w tym na tanycyty, tworząc terapię wielotorową.
- Indywidualizacja podejścia – niektórzy pacjenci mogą mieć silniej zaburzoną funkcję tanycytów, co w przyszłości mogłoby wpływać na dobór konkretnego leczenia.
Dla lekarzy rodzinnych i neurologów taka wiedza to przypomnienie, że proces neurodegeneracyjny nie jest jednoliniowy. Na każdym jego etapie w grę wchodzą różne typy komórek, różne szlaki metaboliczne i różne punkty, w które da się uderzyć terapią.
Co ta praca mówi o profilaktyce i stylu życia
Choć sama publikacja skupia się na mechanizmach komórkowych, trudno uciec od pytania, czy i jak styl życia może wpływać na komórki takie jak tanycyty. Już wcześniej sugerowano, że podwzgórze – rejon, w którym się znajdują – bardzo wrażliwie reaguje na otyłość, przewlekły stres, zaburzenia snu i stany zapalne związane z dietą bogatą w cukier i tłuszcze trans.
Jeżeli regiony mózgu zaangażowane w regulację metabolizmu i hormonów są przeciążone przez lata, cały ekosystem neuronów i komórek glejowych może gorzej radzić sobie z dodatkowymi wyzwaniami, takimi jak toksyczne białka.
Z perspektywy osoby, która myśli o własnym ryzyku demencji, ma to prosty przekaz: dbanie o serce, wagę, poziom cukru we krwi i sen to jednocześnie dbanie o struktury mózgu, które mogą kiedyś stanowić ostatnią linię obrony przed procesami prowadzącymi do otępienia.
Jak rozumieć znaczenie takich badań jako pacjent
Nowe mechanizmy często brzmią abstrakcyjnie: nazwy komórek, białek, receptorów. W praktyce chodzi o to, że nauka coraz dokładniej rozrysowuje „mapę” tego, co dzieje się w mózgu wiele lat przed pierwszymi objawami. To pozwala:
- lepiej tłumaczyć, dlaczego u jednych osób choroba postępuje szybciej, a u innych wolniej,
- szukać okna czasowego, gdy ingerencja daje jeszcze największą szansę na spowolnienie zmian,
- powiązać dane z badań obrazowych, płynu mózgowo-rdzeniowego i krwi z konkretnymi procesami komórkowymi.
W miarę jak takich danych przybywa, neurolog, patrząc na wyniki pacjenta, może coraz precyzyjniej określić, na jakim etapie choroby znajduje się mózg i jaki typ terapii ma sens. Nawet jeśli dziś nie ma w pełni skutecznych leków, to właśnie tak rodzi się medycyna, która za kilka–kilkanaście lat może wyglądać zupełnie inaczej niż dziś.
Tanycyty, o których większość studentów medycyny ledwo słyszała, niespodziewanie trafiły do pierwszego szeregu badań nad demencją. To pokazuje, że w mózgu wciąż czeka wiele nieoczywistych elementów układanki, a każdy z nich może kiedyś przesądzić o tym, czy u konkretnej osoby uda się zatrzymać proces neurodegeneracyjny zanim dojdzie do nieodwracalnych strat.