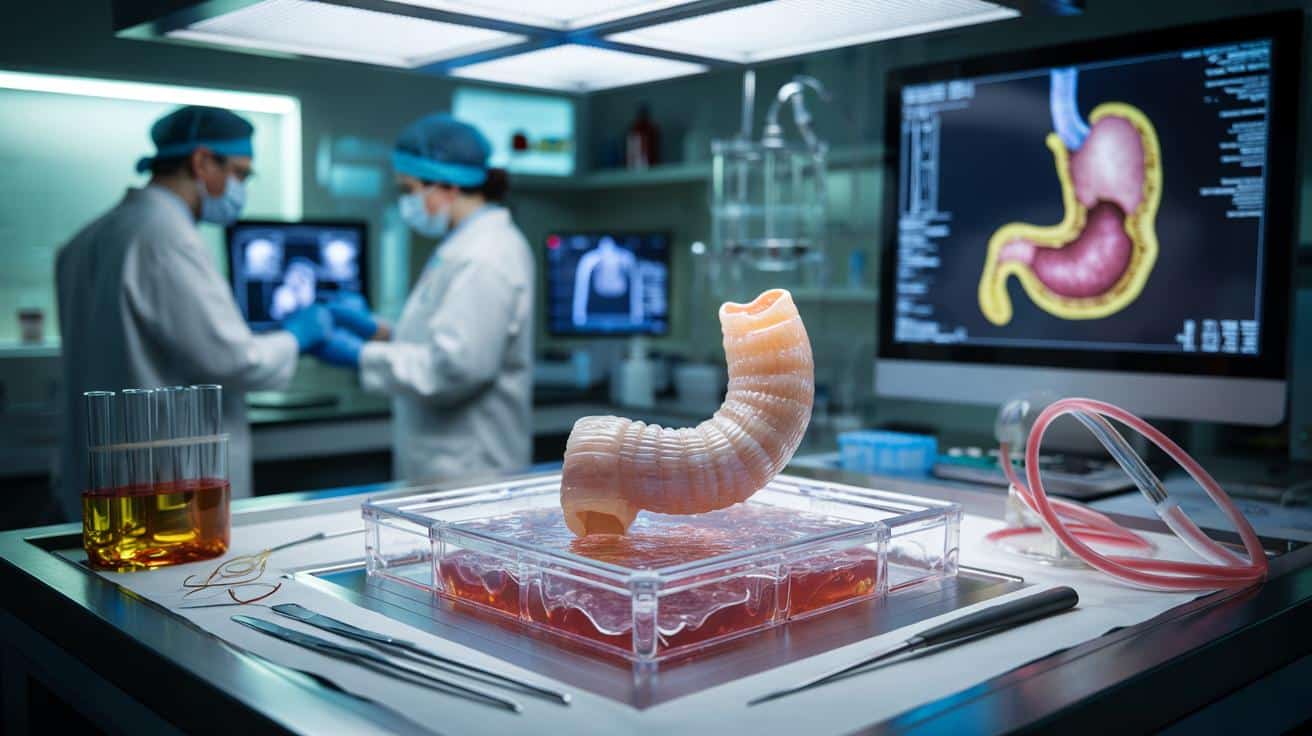
Przełom w medycynie: naukowcy wyhodowali w laboratorium działający fragment przełyku
To, co jeszcze niedawno wydawało się wizją z filmów science fiction, staje się faktem na naszych oczach. Zespół badawczy z Londynu dokonał milowego kroku, tworząc w laboratorium w pełni funkcjonalny fragment przełyku, który pomyślnie przeszedł testy transplantacyjne. Ta innowacyjna technika otwiera zupełnie nowy rozdział w leczeniu skomplikowanych urazów i wad rozwojowych, dając nadzieję pacjentom, dla których medycyna nie miała dotąd idealnych rozwiązań.
Najważniejsze informacje:
- Naukowcy z UCL stworzyli żywy, funkcjonalny odcinek przełyku przy użyciu macierzy pozakomórkowej świni.
- Implanty są personalizowane – wykorzystują komórki pobrane bezpośrednio od pacjenta, co minimalizuje ryzyko odrzutu.
- Badania na miniaturowych świniach potwierdziły, że sztuczny organ integruje się z ciałem i pełni swoje funkcje przez co najmniej pół roku.
- Nowa technologia pozwala na wzrost implantu wraz z dzieckiem, co jest kluczowe w leczeniu wad wrodzonych.
- Pierwsze testy kliniczne na ludziach mogą rozpocząć się w ciągu najbliższych 3-4 lat.
Brzmi jak science fiction, ale to już rzeczywistość: brytyjski zespół badawczy stworzył w laboratorium żywy, funkcjonalny odcinek przełyku z tkanek świń i skutecznie go przeszczepił. Taka technika może w przyszłości zmienić leczenie ciężkich wad wrodzonych i skomplikowanych urazów u dzieci oraz dorosłych.
Dlaczego naprawa przełyku jest tak trudna
Przełyk to nie tylko „rurka”, która łączy gardło z żołądkiem. To dynamiczny narząd, który musi:
- koordynować skurcze mięśni, aby przesuwać kęs jedzenia w dół,
- przewodzić impulsy nerwowe, które sterują tym ruchem,
- wytrzymywać ciągłe rozciąganie i ściskanie podczas połykania,
- zachować szczelność, by treść pokarmowa nie cofała się do góry.
Klasyczne metody rekonstrukcji przełyku są inwazyjne i obarczone powikłaniami. Chirurdzy często muszą wykorzystać fragment jelita lub żołądka, aby zastąpić brakujący odcinek. Taki „zastępczy” fragment nie zawsze pracuje jak prawdziwy przełyk, a dzieci z długoodcinkową atrezją przełyku spędzają miesiące w szpitalach, przechodząc kolejne operacje.
Badacze z Londynu poszli w zupełnie innym kierunku: zamiast przenosić inny narząd, postanowili zbudować przełyk od zera, z komórek biorcy, na zwierzęcej „rusztowaniu” pozbawionym własnych komórek.
Jak powstaje „szkielet” przełyku z tkanki zwierzęcej
Zespół kierowany przez chirurga dziecięcego Paolo De Coppiego z University College London wykorzystał fragment przełyku świni. Najpierw usunięto z niego wszystkie żywe komórki, pozostawiając tylko tzw. macierz pozakomórkową – białkowy szkielet narządu. Taka struktura zachowuje naturalny kształt i warstwową budowę przełyku, ale nie powinna wywoływać silnej reakcji immunologicznej.
Następnie w ten „goły” szkielet wstrzyknięto komórki mięśniowe pobrane od konkretnych świń, które miały otrzymać przeszczep. Naukowcy przeprogramowali je w kierunku komórek o właściwościach zbliżonych do komórek macierzystych, zdolnych tworzyć różne typy tkanek potrzebnych w przełyku.
Tak przygotowany fragment umieszczono w bioraktorze – specjalnym urządzeniu, które kontroluje przepływ płynów, temperaturę i warunki potrzebne do wzrostu tkanek. Tam przez tydzień komórki przyczepiały się do rusztowania i organizowały w bardziej uporządkowaną tkankę. Cała procedura, od pobrania narządu do gotowego przeszczepu, trwała około dwóch miesięcy.
Około dwumiesięczne oczekiwanie na taki implant jest zgodne z realnymi możliwościami leczenia dzieci z długoodcinkową atrezją przełyku, u których planuje się rozbudowane zabiegi rekonstrukcyjne.
Eksperyment na mini-świniach: czy sztuczny przełyk zadziała w żywym organizmie
Aby sprawdzić, czy nowy przełyk potrafi realnie pracować w ciele, naukowcy przeprowadzili serię transplantacji u ośmiu miniaturowych świń ważących około 10 kilogramów. Chirurdzy wycięli u każdego zwierzęcia fragment przełyku o długości 2,5 centymetra i zastąpili go przygotowanym w laboratorium implantem.
Każdy przeszczep owinięto biodegradowalną siatką. Pełniła ona podwójną rolę: stabilizowała miejsce zespolenia i zachęcała organizm do tworzenia nowych naczyń krwionośnych, które miały odżywiać tkankę.
Co działo się po zabiegu
Według danych opisanych w czasopiśmie naukowym Nature Biotechnology wszystkie osiem zwierząt przeszło pierwsze trzydzieści dni po transplantacji bez ciężkich komplikacji. To okres, w którym nowe naczynia krwionośne dopiero się tworzą, a ryzyko martwicy tkanki jest najwyższe.
W kolejnych miesiącach badacze regularnie oceniali:
- czy zwierzęta mogą samodzielnie połykać,
- jak wygląda przepływ pokarmu do żołądka w badaniach obrazowych,
- czy w miejscu przeszczepu pojawia się zwężenie,
- jak zachowuje się nowa tkanka pod mikroskopem.
Po pół roku pięć świń nadal żyło i normalnie jadło, a wszczepiony odcinek przełyku wykazywał prawidłowe skurcze mięśniowe, sieć naczyń oraz unerwienie. Trzy pozostałe zwierzęta uśpiono wcześniej z przyczyn związanych z dobrostanem, co jest standardową procedurą w badaniach przedklinicznych.
Badacze zaobserwowali, że w ciągu trzech miesięcy implant w pełni zintegrował się z otaczającą tkanką i wytwarzał ciśnienie wystarczające do transportu pokarmu do żołądka.
U części świń w miejscu przeszczepu rozwinęły się zwężenia, które utrudniały połykanie. Zespoły medyczne poradziły sobie z nimi za pomocą endoskopowego poszerzania, czyli tej samej metody, jaką stosuje się już dzisiaj u ludzi w przypadku blizn i zwężeń przełyku.
Droga do zastosowania u dzieci i dorosłych
Choć wyniki u miniaturowych świń wyglądają obiecująco, przełożenie tej techniki na ludzi wymaga jeszcze wielu kroków. Zespół pracuje przede wszystkim nad wydłużeniem przeszczepianego fragmentu do 10–15 centymetrów. Taki odcinek byłby już przydatny w leczeniu najtrudniejszych przypadków wrodzonej atrezji przełyku czy rozległych uszkodzeń po połknięciu żrących substancji.
Największe wyzwanie: dopływ krwi
Im dłuższy fragment przełyku, tym trudniej zaopatrzyć go w stabilną sieć naczyń. Bez stałego dopływu krwi komórki obumierają, a implant traci funkcję. Dlatego badacze:
- modyfikują strukturę zwierzęcego rusztowania, aby ułatwić tworzenie naczyń,
- testują różne techniki „zaszczepiania” naczyń jeszcze w bioraktorze,
- analizują, jaką długość przeszczepu organizm jest w stanie realnie ukrwawić.
Równolegle zespół standaryzuje proces produkcji tak, aby ograniczyć liczbę ręcznych kroków, które zwiększają ryzyko błędów i zanieczyszczeń. Docelowo w bankach tkanek miałyby czekać gotowe, odkomórkowane fragmenty przełyku pochodzenia zwierzęcego, które lekarze „uzupełnialiby” już tylko komórkami konkretnego pacjenta.
Personalizowany implant z własnych komórek pacjenta zmniejsza ryzyko odrzutu i może rosnąć wraz z dzieckiem, co ma ogromne znaczenie w chirurgii dziecięcej.
Paolo De Coppi szacuje, że jeśli kolejne badania na zwierzętach potwierdzą bezpieczeństwo i skuteczność tej metody, pierwsze testy kliniczne u dzieci mogłyby wystartować w ciągu około trzech–czterech lat.
Kto może skorzystać z takiej technologii
Adresatami przyszłych terapii nie będą wyłącznie noworodki z wadą wrodzoną przełyku. Na horyzoncie pojawia się szansa także dla innych grup chorych, u których klasyczne zabiegi są szczególnie obciążające.
| Grupa pacjentów | Potencjalne zastosowanie wyhodowanego przełyku |
|---|---|
| Dzieci z długoodcinkową atrezją przełyku | Zastąpienie brakującego odcinka narządu fragmentem rosnącym razem z nimi |
| Dorośli po rozległych operacjach z powodu raka | Odbudowa usuniętego fragmentu bez konieczności przemieszczania żołądka czy jelit |
| Osoby po połknięciu substancji żrących | Rekonstrukcja zniszczonego odcinka z użyciem tkanek pochodzących z ich własnych komórek |
Taka metoda miała by szansę ograniczyć liczbę powikłań, jak refluks, trudności z połykaniem czy liczne zwężenia wymagające powtarzanych zabiegów endoskopowych. Dla części pacjentów mogłaby też oznaczać krótszy pobyt w szpitalu i szybszy powrót do normalnego jedzenia.
Co oznacza „żywy” sztuczny narząd w praktyce
W przeciwieństwie do klasycznych protez, bioinżynieryjny przełyk jest żywą tkanką. To daje kilka istotnych konsekwencji. Implant może goić się tak jak naturalna część organizmu, adaptować się do wzrostu dziecka, a teoretycznie także regenerować po drobnych urazach. Równocześnie wymaga czułego monitorowania – lekarze muszą obserwować, czy mięśnie kurczą się prawidłowo, czy unerwienie działa i czy nie pojawiają się patologiczne blizny.
Warto też pamiętać, że badania te wpisują się w szerszy trend medycyny regeneracyjnej, który stara się naprawiać uszkodzone narządy zamiast je tylko zastępować. Podobne podejścia testuje się m.in. w przypadku tchawicy, pęcherza moczowego czy fragmentów jelita.
Dla pacjentów i ich rodzin ważne będzie też zrozumienie, czym różni się taki przeszczep od klasycznej transplantacji. Z uwagi na użycie własnych komórek chorego, zapotrzebowanie na agresywne leczenie immunosupresyjne może się zmniejszyć. To z kolei oznacza mniejsze ryzyko infekcji i powikłań związanych z tłumieniem odporności.
Jeżeli kolejne badania potwierdzą bezpieczeństwo tej metody, lekarze staną przed nowym zestawem pytań: jak kwalifikować pacjentów, kiedy najlepiej wykonać zabieg, jakie badania kontrolne prowadzić przez kolejne lata. Zmieni się nie tylko sam zabieg chirurgiczny, ale cała ścieżka opieki nad dzieckiem lub dorosłym z ciężkim uszkodzeniem przełyku.
Najczęściej zadawane pytania
Jak powstaje wyhodowany w laboratorium przełyk?
Proces polega na usunięciu komórek z tkanki zwierzęcej i zasiedleniu pozostałego 'szkieletu’ białkowego komórkami mięśniowymi pacjenta w specjalnym bioreaktorze.
Kto najbardziej skorzysta na tej nowej technologii?
Głównymi adresatami są dzieci z wrodzoną atrezją przełyku, dorośli po operacjach nowotworowych oraz osoby po oparzeniach chemicznych.
Dlaczego ta metoda jest lepsza od tradycyjnych przeszczepów?
Użycie własnych komórek pacjenta drastycznie zmniejsza ryzyko odrzutu i eliminuje potrzebę stosowania silnych leków immunosupresyjnych.
Kiedy nowa metoda trafi do szpitali?
Jeśli dalsze testy zakończą się sukcesem, pierwsze próby kliniczne z udziałem dzieci mogą ruszyć za około 3 do 4 lat.
Wnioski
Sukces brytyjskich badaczy to jasny sygnał, że era 'drukowania’ organów na wymiar jest bliżej niż myślimy. Dla pacjentów oznacza to mniej bolesnych operacji i życie bez konieczności przyjmowania obciążających leków przeciw odrzutom. Choć na powszechną dostępność tej metody musimy jeszcze poczekać kilka lat, warto śledzić rozwój medycyny regeneracyjnej, która zaczyna realnie naprawiać ludzkie ciało zamiast tylko łatać jego ubytki.
Podsumowanie
Brytyjscy naukowcy z sukcesem wyhodowali i przeszczepili funkcjonalny fragment przełyku stworzony z komórek biorcy na zwierzęcym rusztowaniu. Ta pionierska metoda medycyny regeneracyjnej może wkrótce zrewolucjonizować leczenie wad wrodzonych oraz poważnych urazów u dzieci i dorosłych.